马玉虹医生的科普号
- 精选 肝硬化患者“不拘小节”,需警惕“肝昏迷”
老陈患乙肝肝硬化多年了,春节期间全家其乐融融,也没有像平常那样注意节制饮食,大鱼大肉多吃了些,细心的家人发现他话多了,睡眠少了,还随地吐痰,乱扔垃圾,不拘小节,这可急坏了家人,情急之下赶紧叫来救护车把老陈送到长沙市第一医院南院(长沙市传染病医院)。经医院肝病专家诊断后,认为他得的是肝性脑病,俗称“肝昏迷”,需赶紧救治,不然恐有生命之忧。专家介绍:肝性脑病又称肝昏迷,是严重肝病或终末期肝硬化引起的、以代谢紊乱为基础的中枢神经系统功能失调综合病征。肝性脑病的常见诱因包括上消化道出血、感染、电解质紊乱、手术创伤、蛋白饮食摄入过多等。发病机制目前尚不明了。肝性脑病起病可急可缓。重型肝炎/肝衰竭起病急,病情变化快,患者可迅速进入昏迷,多伴有黄疸出现,急性重型肝炎可在黄疸出现前即可表现行为意识障碍,有的甚至被误以为是精神病;亚急性和慢性重型肝炎者肝性脑病相对起病隐匿,由于症状缺乏特异性,疾病初期常不易发现,往往发生误诊和漏诊贻误抢救时机。肝病患者如有以下症状时需警惕肝性脑病:肝病患者性格改变可能是本病最早出现的症状,原属外向型性格者可表现为抑郁,而原属内向型性格者表现为欣快多语;行为改变最初可能仅限于一些“不拘小节”的行为,如乱写乱画,乱洒水,乱吐痰,乱扔纸屑、烟头,乱摸乱寻、随地大小便、房间内的桌椅随意乱拖乱放等不自主行为;睡眠习惯改变:常表现为睡眠生物钟倒错,白天昏昏欲睡,晚上则欣快不己,常预示肝性脑病先兆;肝臭的出现:患者经肺呼出或经皮肤散发出一股难以言状的特殊气味,被医生称之为"肝臭";扑翼样震颤:是疾病初期具特征性的神经系统表现,有早期诊断肝性脑病的意义:做法是医生嘱病人双眼紧闭,伸出前臂,张开五指或腕部过度伸展并固定不动时,病人掌-指及腕关节可出现快速的屈曲及伸展运动,每秒钟常可出现1~2次,也有达每秒钟5~9次者,病情进一步加重时患者可出现计算力和定向力的障碍甚至昏迷不醒。肝昏迷是终末期肝硬化、重型肝炎、肝癌等肝病晚期的常见严重并发症,如诊断抢救不及时可迅速导致患者死亡。晚期肝硬化病人肝脏处理蛋白质的能力下降,一次或短期内过多食用高蛋白食物,可导致血液中氨类等有毒物质急骤升高发生肝性脑病。医生对老陈实施控制蛋白质饮食,并通过血液净化及对症治疗后,病情很快得到了控制,目前身体在进一步的恢复当中。医生告知患者家属:"老陈因患晚期肝硬化,不宜过多食用蛋白质饮食,过节期间短期内过多的蛋白质饮食是老陈发生肝昏迷的罪魁祸首"!专家呼吁:晚期肝硬化患者及家人都应提高认识、积极做好防范措施,合理均衡饮食及营养,特别时逢节假日,更应严防饮食不当诱发肝昏迷的发生。饮食中富含蛋白质的食物如鸡蛋、牛奶、奶酪、瘦肉、鱼肉、鸡肉等可交替食用,医生建议此类肝病患者少吃多餐为宜,强调控制每日蛋白质总量。发生肝性脑病时应及时就医,在医生的指导干预下积极救治并合理饮食。 作者:李金强 尹梅影
5024人已读 - 精选 肿瘤患者冬季饮食
肿瘤患者在冬季应该如何进补呢? 2016-11-11 西京医院消化季刚 肿瘤免疫细胞治疗资讯 冬季气候寒冷,肿瘤患者需要保持一定的热量抵御寒冷,同时又要避免高蛋白、高脂肪饮食,所以,肿瘤患者在冬季应该如何进补显得尤为重要。肿瘤患者冬天进补要遵循“低脂肪、少量优质蛋白质和高碳水化合物”的总体原则。 1、多吃主食,适当吃低脂肪、优质蛋白食物。 蛋白质、脂肪和碳水化合物被称为产热营养素。但大量蛋白、脂肪的摄入会增加包括肝脏、胰腺等器官在内的消化系统的负担。因此,低脂肪、少量优质蛋白质的饮食结构特别适合肿瘤患者尤其是肝癌、胰腺癌的患者。含有优质蛋白低脂肪的食物日常生活中较多见的有鲤鱼、虾、蛤肉、蟹肉、牡蛎、鹌鹑蛋、木耳及各种豆制品等。另外,没有糖尿病的肿瘤患者也可以吃蜂蜜、马铃薯等含糖较多的食物以补充热量。 2、宜食温热性并含钾、钙的食物。 寒冷会影响人体的泌尿系统,导致排尿增多,随尿排出的钠、钾、钙等无机盐也较多。钠可以从食盐中获取,钾、钙则主要来自其他食物。因此,冬天进补时,应该多吃含钾、钙等无机盐较多的食物,例如多吃一些香菇、芋头、板栗、桂圆、南瓜等温热性质的食物。香蕉虽然含钾较多,但性质寒凉,冬天不宜多食。 3、增加维生素A、C的摄取。 增加维生素A、C的摄取,也可以增强对寒冷的适应能力,而维生素A主要多来自胡萝卜、深绿色蔬菜等;维生素C则主要来自于新鲜水果和蔬菜。 4、芝麻、葵花子能提供人体耐寒的必要元素。 寒冷天气使人体对蛋氨酸的需求量增大。蛋氨酸可以通过转移作用,提供一系列适应寒冷所必需的甲基。因此,冬季应多摄取含蛋氨酸较多的食物。如芝麻、葵花子、乳制品、酵母、叶类蔬菜等。 总之,肿瘤患者冬天进补应遵循“低脂肪、少量优质蛋白质和高碳水化合物”的总体原则,宜少食用寒凉食物,适量补充钾、钙等无机盐及维生素,增强体质。
孙冰生 主任医师 天津医科大学肿瘤医院 肺部肿瘤科3472人已读 - 精选 最新原发性肝癌诊疗规范(2017年版)
一、概述原发性肝癌是目前我国第四位的常见恶性肿瘤及第三位的肿瘤致死病因,严重威胁我国人民的生命和健康1,2。原发性肝癌主要包括肝细胞癌(Hepatocellular Carcinoma,HCC)、肝内胆管癌(Intrahepatic Cholangiocarcinoma,ICC)和HCC-ICC混合型三种不同病理类型,三者在发病机制、生物学行为、组织学形态、治疗方法以及预后等方面差异较大,其中肝细胞癌占到85%-90%以上,因此本规范中的“肝癌”指肝细胞癌。二、筛查和诊断(一)高危人群的监测筛查:对肝癌高危人群的筛查,有助于早期发现、早期诊断、早期治疗,是提高肝癌疗效的关键。在我国,肝癌的高危人群主要包括:具有乙型肝炎病毒(Hepatitis B virus,HBV)和/或丙型肝炎病毒(Hepatitis C virus,HCV)感染、长期酗酒、非酒精脂肪性肝炎、食用被黄曲霉毒素污染食物、各种原因引起的肝硬化、以及有肝癌家族史等的人群,尤其是年龄40岁以上的男性风险更大。血清甲胎蛋白(Alpha-fetoprotein,AFP)和肝脏超声检查是早期筛查的主要手段,建议高危人群每隔6个月进行至少一次检查3。(二)肝癌的影像学检查:各种影像学检查手段各有特点,应该强调综合应用、优势互补、全面评估。1. 超声检查(Ultrasonography, US):腹部超声检查因操作简便、灵活直观、无创便携等特点,是临床上最常用的肝脏影像学检查方法。常规超声筛查可以早期、敏感地检出肝内可疑占位性病变,准确鉴别是囊性或实质性占位,并观察肝内或腹部有无其他相关转移灶。彩色多普勒血流成像不仅可以观察病灶内血供,也可明确病灶与肝内重要血管的毗邻关系,为临床治疗方法的选择及手术方案的制定提供重要信息。实时超声造影技术可以揭示肝肿瘤的血流动力学改变,帮助鉴别和诊断不同性质的肝肿瘤,凭借实时显像和多切面显像的灵活特性,在评价肝肿瘤的微血管灌注和引导介入治疗方面具有优势。2. X线计算机断层成像(Computed Tomography, CT):常规采用平扫+增强扫描方式(常用碘对比剂),其检出和诊断小肝癌能力总体略逊于磁共振成像。目前除常见应用于肝癌临床诊断及分期外,更多应用于肝癌局部治疗的疗效评价,特别对经肝动脉化疗栓塞(Transarterial chemoembolization,TACE)后碘油沉积观察有优势。同时,借助CT的三维肝体积和肿瘤体积测量、肺和骨等其它脏器转移评价,临床应用广泛。3. 磁共振成像(Magnetic Resonance Imaging, MRI):常规采用平扫+增强扫描方式(常用对比剂Gd-DTPA),因其具有无辐射影响,组织分辨率高,可以多方位、多序列参数成像,并具有形态结合功能(包括弥散加权成像、灌注加权成像和波谱分析)综合成像技术能力,成为临床肝癌检出、诊断和疗效评价的常用影像技术。若结合肝细胞特异性对比剂(Gd-EOB-DTPA)使用,可提高≤1.0cm肝癌的检出率和对肝癌诊断及鉴别诊断的准确性4-9。在MRI或 CT增强扫描动脉期(主要在动脉晚期),肝癌呈不均匀明显强化,偶可呈均匀明显强化,尤其是≤5.0cm的肝癌,门脉期和/或实质平衡期扫描肿瘤强化明显减弱或降低,这种“快进快出”的增强方式是肝癌诊断的特点10,11。肝癌MRI和CT诊断,尚需结合其它征象(如假包膜等),尤其是MRI其它序列上相关征象进行综合判断,方能提高肝癌诊断准确性。4.数字减影血管造影(Digital Subtraction Angiography, DSA): DSA是一种侵入性创伤性检查,多主张采用经选择性或超选择性肝动脉进行DSA检查,该技术更多用于肝癌局部治疗或急性肝癌破裂出血治疗等。肝癌在DSA的主要表现是肿瘤血管和肿瘤染色,还可以明确显示肝肿瘤数目、大小及其血供情况。DSA能够为血管解剖变异和重要血管解剖关系以及门静脉浸润提供正确客观的信息,对于判断手术切除的可能性和彻底性以及决定合理的治疗方案有重要价值。5.核医学影像检查:(1)正电子发射计算机断层成像(Positron Emission Tomography/CT, PET/CT) :氟-18-脱氧葡萄糖(18F-FDG)PET/CT全身显像的优势在于:①对肿瘤进行分期,通过一次检查能够全面评价淋巴结转移及远处器官的转移12,13(证据等级1);②再分期,因PET功能影像不受解剖结构的影响,可准确显示解剖结构发生变化后或者是解剖结构复杂部位的复发转移灶14,15(证据等级2);③疗效评价,对于抑制肿瘤活性的靶向药物,疗效评价更加敏感、准确16,17(证据等级2);④指导放疗生物靶区的勾画、穿刺活检部位14,15(证据等级2);⑤评价肿瘤的恶性程度和预后18-20(证据等级2)。碳-11标记的乙酸盐(11C-acetate)或胆碱(11C-choline)PET显像可提高对高分化肝癌诊断的灵敏度,与18F-FDG PET/CT显像具有互补作用21,22。(2)发射单光子计算机断层扫描仪(SPECT-CT): SPECT/CT已逐渐替代SPECT成为核医学单光子显像的主流设备,选择全身平面显像所发现的病灶,再进行局部SPECT/CT融合影像检查,可同时获得病灶部位的SPECT和诊断CT图像,诊断准确性得以显著提高23。6. 肝穿刺活检:具有典型肝癌影像学特征的占位性病变,符合肝癌的临床诊断标准的病人,通常不需要以诊断为目的肝穿刺活检24。对于缺乏典型肝癌影像学特征的占位性病变,肝穿刺活检可获得病理诊断,对于确立肝癌的诊断、指导治疗、判断预后非常重要。肝穿刺活检需要在超声或CT引导下进行,可采用18G或16G肝穿刺空芯针活检获得组织学诊断,也可用细针穿刺获得细胞学诊断。肝穿刺活检主要的风险是出血或针道种植。因此,术前应检查血小板和凝血功能,对于有严重出血倾向或严重心肺、脑、肾疾患和全身衰竭的病人,应避免肝穿刺活检。为了避免肿瘤结节破裂和针道种植,在选择穿刺路径需要经过正常的肝组织,避免直接穿刺肝脏表面的结节。推荐在肿瘤和肿瘤旁肝组织分别穿刺1条组织,以便客观对照提高诊断准确性。肝穿刺的病理诊断存在一定的假阴性率,阴性结果不能完全排除肝癌的可能。(三)肝癌的血清学分子标记物:血清甲胎蛋白(Alpha-fetoprotein, AFP)是当前诊断肝癌常用而又重要的方法。诊断标准:AFP≥400μg/L,排除慢性或活动性肝炎、肝硬化、睾丸或卵巢胚胎源性肿瘤以及怀孕等。AFP低度升高者,应作动态观察,并与肝功能变化对比分析,有助于诊断。约30%的肝癌病人AFP水平正常,检测甲胎蛋白异质体,有助于提高诊断率25。其它常用的肝癌诊断分子标志物:包括α-L-岩藻苷酶、异常凝血酶原等。(四)肝癌的病理学诊断:(五)肝癌的临床诊断标准及路线图:乙型或丙型肝炎以及肝硬化是肝癌的高危因素,对于肝脏占位性病变的诊断和鉴别诊断有重要的价值。近年来,非酒精性脂肪性肝炎(NASH)与肝癌的关系越来越引起重视。——AFP在缺乏敏感的影像学方法情况下曾用于肝癌的临床诊断,如果AFP≥400μg/L,在排除妊娠、慢性或活动性肝病以及生殖腺胚胎源性肿瘤情况下,则高度提示肝癌。结合肝癌发生的高危因素、影像学特征以及血清学分子标记物,依据路线图的步骤对肝癌做出临床诊断(参见附录四)。1. 有乙型肝炎或丙型肝炎,或者有任何原因引起肝硬化者,至少每隔6个月进行一次超声及AFP检测,发现肝内直径≤2cm结节,动态增强MRI、动态增强CT、超声造影及普美显动态增强MRI四项检查中至少有两项显示有动脉期病灶明显强化、门脉或延迟期强化下降的“快进快出”的肝癌典型特征,则可做出肝癌的临床诊断;对于发现肝内直径>2cm的结节,则上述四种影像学检查中只要有一项有典型的肝癌特征,即可临床诊断为肝癌。2. 有乙型肝炎或丙型肝炎,或者有任何原因引起肝硬化者,随访发现肝内直径≤2cm结节,若上述四种影像学检查中无或只有一项检查有典型的肝癌特征,可进行肝穿刺活检或每2-3个月密切的影像学随访以确立诊断;对于发现肝内直径>2cm的结节,上述四种影像学检查无典型的肝癌特征,则需进行肝穿刺活检以确立诊断。3. 有乙型肝炎或丙型肝炎,或者有任何原因引起肝硬化者,如AFP升高,特别是持续增高,应该进行上述四种影像学检查以确立肝癌的诊断,如未发现肝内结节,在排除妊娠、活动性肝病、生殖胚胎源性肿瘤以上消化道癌的前提下,应该密切随访AFP水平以及每隔2-3个月一次的影像学复查。三、分期肝癌的分期对于预后的评估、合理治疗方案的选择至关重要。影响肝癌病人预后的因素很多,包括肿瘤因素、病人一般情况及肝功能情况,据此国外有多种的分期方案,如:BCLC、TNM、JSH、APASL等分期。依据中国的具体国情及实践积累,推荐下述肝癌的分期方案,包括:Ia期、Ib期、IIa期、IIb期、IIIa期、IIIb期、IV期,具体分期方案参见附录五。四、治疗肝癌治疗领域的特点是多种方法、多个学科共存,而以治疗手段的分科诊疗体制与实现有序规范的肝癌治疗之间存在一定的矛盾。因此肝癌诊疗须重视多学科诊疗团队的模式,从而避免单科治疗的局限性,为病人提供一站式医疗服务、促进学科交流,并促进建立在多学科共识基础上的治疗原则和指南。合理治疗方法的选择需要有高级别循证依据支持,但也需要同时考虑地区和经济水平差异。(一)肝切除术:肝癌的外科治疗是肝癌病人获得长期生存最重要的手段,主要包括肝切除术和肝移植术。1.肝切除术的基本原则:(1)彻底性:完整切除肿瘤,使切缘无残留肿瘤;(2)安全性:保留有足够功能肝组织(具有良好血供以及良好的血液和胆汁回流)以术后肝功能代偿,降低手术死亡率及手术并发症。2.术前肝功能储备的评估:在术前应对病人的全身情况及肝功能储备进行全面评价:常采用美国东部肿瘤协作组提出的功能状态评分(ECOG PS)来评估病人的全身情况;采用Child-Pugh评分、吲哚氰绿(ICG)清除试验37或瞬时弹性成像测定肝脏硬度37-40评价肝功能储备情况;如预期保留肝组织体积较小,则采用CT和/或MRI测定剩余肝的体积,并计算剩余肝体积占标准化肝脏体积的百分比38。一般认为Child-Pugh A级、ICG15<20%-30%是实施手术切除的必要条件;余肝体积须占标准肝体积的40%以上(肝硬化病人),或30%以上(无肝硬化病人)也是实施手术切除的必要条件。3.肝癌切除的适应证:(1)肝脏储备功能良好的Ia期、Ib期和IIa期肝癌是手术切除的首选适应证,尽管有以往研究显示对于直径≤3cm肝癌,切除和射频消融疗效无差异41(证据等级1),但最近的研究显示外科切除的远期疗效更好42-44(证据等级1)。(2)在部分IIb期和IIIa期肝癌病人中,手术切除有可能获得比其他治疗方式更好的效果45,46(证据等级1),但需更为谨慎的术前评估。对于多发性肝癌,相关研究显示,在满足手术安全性的条件下,肿瘤数目≤3枚的多发性肝癌病人可能从手术获益45,47(证据等级1);若肿瘤数目>3枚,即使已手术切除,在多数情况下其疗效也并不优于TACE等非手术治疗。(3)对于其它IIb期和IIIa期肝癌,如有以下情况也可考虑手术切除,如肿瘤数目>3枚,但肿瘤局限在同一段或同侧半肝者,或可同时行术中射频消融处理切除范围外的病灶;合并门静脉主干或分支癌栓者,若肿瘤局限于半肝,且预期术中癌栓可完整切除或取净,可考虑手术切除肿瘤并经门静脉取栓,术后再结合TACE、门静脉化疗或其他全身治疗措施;如合并胆管癌栓且伴有梗阻性黄疸,肝内病灶亦可切除的病人;伴有肝门部淋巴结转移者,切除肿瘤的同时行淋巴结清扫或术后外放射治疗;周围脏器受侵犯,但可一并切除者。此外,对于术中探查不适宜切除的肝癌,可考虑术中肝动脉结扎(已少用,有时用于肝癌破裂出血时的手术止血)和(或)肝动脉、门静脉插管化疗、或术中其他的局部治疗措施等。4. 肝癌根治性切除标准:(1)术中判断标准:①肝静脉、门静脉、胆管以及下腔静脉未见肉眼癌栓;②无邻近脏器侵犯,无肝门淋巴结或远处转移;③肝脏切缘距肿瘤边界>1cm;如切缘< 1cm,但切除肝断面组织学检查无肿瘤细胞残留,即切缘阴性。(2)术后判断标准:①术后2个月行超声、CT、MRI(必须有其中两项)检查未发现肿瘤病灶;②如术前AFP 升高,则要求术后2个月AFP 定量测定,其水平在正常范围(极个别病人AFP降至正常的时间超过2个月)。5.手术切除技术:常用的肝切除主要是包括入肝和出肝血流控制技术、肝脏离断技术以及止血技术。手术技术方面,有经验的医师可开展腹腔镜或机器人辅助微创肝切除术。微创手术具有创伤小和术后恢复快等优点48(证据等级2),但其长期疗效仍需要与传统的开腹手术进行前瞻性的多中心的随机对照研究。经腹腔镜行肝癌切除的指征:①病变位于CouinaudII、III、IVb、V、VI段;②病变大小以不影响第一和第二肝门的解剖为准,一般不超过10cm;③有丰富经验的医师可逐步开展腹腔镜半肝切除、肝3叶切除和CouinaudI、VII、VIII段肝切除。切除范围较大导致余肝体积过少或顾忌余肝的功能,是阻碍根治性切除的主要原因。为了提高肝癌的可切除性,可采用如下方法:(1)术前TACE可使部分病人的肿瘤缩小后再切除49,50;(2)经门静脉栓塞(Portal vein thrombosis,PVE)或门静脉结扎(Portal vein ligation,PVL)主瘤所在半肝,使余肝代偿性增大后再切除51。临床报告其并发症不多,因需4-6周时间等待对侧肝组织体积增大,为减少等待期间肿瘤进展的风险,可考虑与TACE联合52。(3)联合肝脏分隔和门静脉结扎的二步肝切除术(Associating liver partition and portal vein ligation for staged hepatectomy,ALPPS)是近年发展的新技术53,,适合于预期残余肝脏体积占标准肝体积不足30%-40%的病人,经过I期的肝脏分隔或离断和患侧门静脉分支结扎后,健侧剩余肝脏体积(future liver reserve, FLR)一般在1-2周后增生30%-70%以上,FLR占标准肝脏体积至少30%以上,可接受安全的II期切除。术前评估非常重要,需要考虑肝硬化的程度、病人年龄、短期承受两次手术的能力和肿瘤快速进展的风险54;此外可借助腹腔镜技术或消融技术等降低二次手术的创伤55。ALPPS的禁忌证:①存在不可切除的肝外转移灶;②严重的门静脉高压症;③全身麻醉高风险病人以及一般状况较差不能耐受大手术的病人;④I期手术后FLR中有肉眼可见肝癌结节。ALPPS应用可在短期内提高肝癌的切除率,但同时也存在高并发症发生率及死亡率,应谨慎、合理地选择手术对象。(4)对于开腹后探查发现肝硬化较重、肿瘤位置深在、多结节的肿瘤,术中消融可降低手术风险。解剖性切除与非解剖性切除均为常用的手术技术。对于巨大肿瘤,可采用不游离肝周韧带的前径路肝切除法56。对于多发性肿瘤,可采用手术切除结合术中消融(如术中射频等)方式治疗,切除肝脏边缘肿瘤,消融深部肿瘤。对于门静脉癌栓者,行门静脉取栓术时应暂时阻断健侧门静脉血流,防止癌栓播散57。对于肝静脉癌栓或腔静脉癌栓者,可行全肝血流阻断,尽可能整块去除癌栓58。合并右心房癌栓者,可开胸切开右心房取出癌栓,同时切除肝肿瘤。合并腔静脉或右心房癌栓时手术风险较大,应慎重选择。对于肝癌伴胆管癌栓者,在去除癌栓的同时,若肿瘤已部分侵犯胆管壁,则应同时切除受累胆管并重建胆道,以降低局部复发率59。6. 术前治疗:对于不可切除肝癌,肝动脉结扎插管、TACE、外放射等治疗可能导致肿瘤降期从而使部分病人获得手术切除的机会,降期后切除的肝癌病人可能获得较好的长期生存效果49。对于可切除肝癌,术前TACE并不能改善病人生存60,61(证据等级2)。7.术后治疗(转移复发的防治):肝癌手术切除后5年肿瘤复发转移率高达40%-70%,这与术前可能已存在微小播散灶或者多中心发生有关,故所有病人术后需要接受密切随访。一旦发现肿瘤复发,根据肿瘤复发的特征,可以选择再次手术切除、局部消融、TACE、放疗或系统治疗等,延长病人生存期。对于高危复发者,有临床研究证实术后TACE治疗有一定的效果,能发现并控制术后肝内微小残癌62(证据等级4),但该结论需要进一步证实。此外,对于伴有门静脉癌栓病人术后经门静脉置管化疗联合肝动脉化疗栓塞,也可延长病人生存63。尽管有临床随机研究提示,干扰素α可减少复发延长生存64-66(证据等级1),但仍存争议67,目前仅推荐应用于合并慢性乙肝背景的肝癌术后病人。有报道发现肝癌miR-26a表达与干扰素α辅助治疗的疗效相关68,该结果也需要进一步多中心随机对照证实。亦有大会报道,国内多中心随机平行对照研究结果表明,中药槐耳颗粒对肝癌根治性切除术后的病人有一定的预防复发转移作用。(二)肝移植术1.肝癌肝移植适应证:肝移植是肝癌根治性治疗手段之一,尤其适用于有失代偿肝硬化背景、不适合切除的小肝癌病人。合适的适应证是提高肝癌肝移植疗效,保证宝贵的供肝资源得到公平合理应用的关键。关于肝移植适应证,国际上主要采用米兰(Milan)标准,美国加州大学旧金山分校(UCSF)标准等。国内尚无统一标准,已有多家单位和学者陆续提出了不同的标准,包括杭州标准71、上海复旦标准72、华西标准73和三亚共识74等。各家标准对于无大血管侵犯、淋巴结转移及肝外转移的要求都比较一致,但是对于肿瘤的大小和数目的要求不尽相同。上述国内标准均不同程度的扩大了肝癌肝移植的适用范围,可使更多的肝癌病人因肝移植手术受益,并未明显降低术后总体生存率和无瘤生存率。但仍需多中心协作研究以支持和证明,从而获得高级别的循证医学证据。经专家组充分讨论,现阶段本规范推荐采用UCSF标准。2.肝癌肝移植术后复发的预防:肝癌肝移植术后的肿瘤复发明显减低了移植后生存率。其危险因素包括肿瘤分期、血管侵犯、AFP水平、免疫抑制剂累积用药剂量量等。减少移植后早期钙调磷酸酶抑制剂的用量可能降低肿瘤复发率75(证据等级2)。肝癌肝移植采用mTOR抑制剂的免疫抑制方案亦可能预防肿瘤复发,提高生存率76,77(证据等级2),但尚需多中心随机临床研究的进一步证实。(三)局部消融治疗尽管外科手术是肝癌的首选治疗方法,但因肝癌病人大多合并有肝硬化,或者在确诊时大部分病人已达中晚期,能获得手术切除机会的病人约20%-30%。近年来广泛应用的局部消融治疗,具有创伤小、疗效确切的特点,使一些不耐受手术切除的肝癌病人亦可获得根治的机会。局部消融治疗是借助医学影像技术的引导对肿瘤靶向定位,局部采用物理或化学的方法直接杀灭肿瘤组织的一类治疗手段。主要包括射频消融(Radiofrequency ablation,RFA)、微波消融(Microwave ablation,MWA)、冷冻治疗、高功率超声聚焦消融(High power focused ultrasound ablation,HIFU)以及无水乙醇注射治疗(Percutaneous ethanol injection,PEI)等。局部消融最常用超声引导,具有方便、实时、高效的特点。CT及MRI结合多模态影像系统可用于观察超声无法探及的病灶。CT及MRI引导技术还可应用于肺、肾上腺、骨等转移灶的消融等。消融的路径有经皮、腹腔镜、或开腹三种方式。大多数的小肝癌可以经皮穿刺消融,具有经济、方便、微创的特点。位于肝包膜下的肝癌,特别是突出肝包膜外的肝癌,经皮穿刺消融风险较大,或者影像学引导困难的肝癌,可考虑经开腹消融和经腹腔镜消融的方法。局部消融治疗适用于单个肿瘤直径≤5cm;或肿瘤结节不超过3个、最大肿瘤直径≤3cm;无血管、胆管和邻近器官侵犯以及远处转移78-80(证据等级1),肝功能分级为Child-Pugh A或B级的肝癌病人,可获得根治性的治疗效果。对于不能手术切除的直径3-7cm的单发肿瘤或多发肿瘤,可联合TACE81,82(证据等级1)。1. 常见消融手段包括:(1)RFA:是肝癌微创治疗的最具代表性消融方式,其优点是操作方便,住院时间短,疗效确切,花费相对较低,特别适用于高龄病人。对于直径≤3cm肝癌病人,RFA的无瘤生存率略逊于手术切除43,78(证据等级1)。与PEI相比,RFA具有根治率高、所需治疗次数少和远期生存率高的显著优势。RFA治疗的精髓是对肿瘤整体灭活并尽量减少正常肝组织损伤,其前提是对肿瘤浸润范围和卫星灶的确认。因此,十分强调治疗前精确的影像学检查。超声造影技术有助于确认肿瘤的实际大小和形态,界定肿瘤浸润范围,检出微小肝癌和卫星灶,为制定消融方案灭活肿瘤提供了可靠的参考依据。(2)MWA:是我国常用的热消融方法,在局部疗效、并发症发生率以及远期生存方面与RFA相比都无显著差异。其特点是消融效率高,避免RFA所存在的“热沉效应”。现在的MWA技术也能一次性灭活肿瘤,血供丰富的肿瘤,可先凝固阻断肿瘤主要滋养血管,再灭活肿瘤,可以提高疗效。建立温度监控系统可以调控有效热场范围,保证凝固效果。随机对照研究显示,两者之间无论是在局部疗效和并发症方面,还是生存率方面都无统计学差异85(证据等级1),MWA和RFA,这两种消融方式的选择可根据肿瘤的大小、位置,选择更适宜的消融方式83(证据等级3)。(3)PEI:适用于直径≤3cm以内肝癌的治疗,局部复发率高于RFA,但PEI对直径≤2cm的肝癌消融效果确切,远期疗效类似于RFA。PEI的优点是安全,特别适用于癌灶贴近肝门、胆囊及胃肠道组织,而热消融治疗(RFA和MWA)可能容易造成损伤的情况下。2. 基本技术要求需要注意以下方面:(1)操作医师必须经过严格培训和足够的实践积累,治疗前应该全面而充分地评估病人的全身状况,肝功能状态,肿瘤的大小、位置、数目等。要注意肿瘤与邻近器官的关系,制定合理的穿刺路径及消融范围,在保证安全的前提下,达到足够的安全范围。(2)根据肿瘤的大小、位置,强调选择适合的影像引导技术(超声或CT)和消融手段(RFA、MWA或PEI)。(3)肿瘤距肝门部肝总管、左右肝管的距离应至少为5mm。不推荐对>5cm的病灶单纯施行消融治疗。对于多个病灶或更大的肿瘤,根据病人肝功能状况,采取治疗前TACE+消融联合治疗,效果优于单纯的消融治疗。(4)消融范围应力求包括5mm的癌旁组织,以获得“安全边缘”,彻底杀灭肿瘤。对于边界不清晰、形状不规则的浸润型癌或转移癌灶,在邻近肝组织及结构条件许可的情况下,建议适当扩大消融范围。3. 对于直径≤5cm的肝癌治疗选择:数项临床前瞻性随机对照和系统回顾性分析显示,手术切除宜首选42-44,78(证据等级1)。在临床实践中,应该根据病人的一般状况和肝功能,肿瘤的大小、数目、位置决定,以及从事消融治疗的医师的技术和经验,全面考虑后选择合适的初始治疗手段。通常认为,如果病人能够耐受肝切除术,以及肝癌位置表浅或位于肝脏边缘,应首选手术切除。局部消融可作为手术切除之外的另一种治疗选择。对于2-3个癌灶位于不同区域、或者位居肝脏深部或中央型≤5cm的肝癌,局部消融可以达到手术切除疗效,获得微创下根治性消融。4. 肝癌消融治疗后应重视的评估和随访:评估局部疗效的规范方法是在消融后1个月左右,复查肝脏动态增强CT或MRI,或者超声造影,以评价消融效果。消融效果可分为:①完全消融(Complete response,CR):经动态增强CT或MRI扫描,或者超声造影随访,肿瘤所在区域为低密度(超声表现为高回声),动脉期未见强化;②不完全消融(In-complete response,ICR):经动态增强CT或MRI扫描,或者超声造影随访,肿瘤病灶内局部动脉期有强化,提示有肿瘤残留。对治疗后有肿瘤残留者,可以进行再次消融治疗;若2次消融后仍有肿瘤残留,视为消融治疗失败,应放弃消融疗法,改用其他疗法。完全消融后应定期随访复查,通常情况下每隔2~3月复查肿瘤标志物、彩超、MRI或CT,以便及时发现可能的局部复发病灶和肝内新发病灶,利用经皮消融微创安全和简便易于反复施行的优点,有效地控制肿瘤进展。(四)TACE治疗TACE治疗在国内亦称介入疗法、介入治疗Interventional treatment ),目前被公认为肝癌非手术治疗的最常用方法之一84-89(证据等级1)。1.基本原则:(1)要求在数字减影血管造影机下进行;(2)必须严格掌握临床适应证;(3)必须强调超选择插管至肿瘤的供养血管内治疗;(4)必须强调保护病人的肝功能;(5)必须强调治疗的规范化和个体化;(6)如经过4-5次TACE治疗后,肿瘤仍继续进展,应考虑换用或联合其它治疗方法,如外科手术、局部消融和系统治疗以及放疗等。2.适应证:(1)IIb期、IIIa期和IIIb期的部分病人,肝功能分级Child-PughA或B级,ECOG评分0-2;(2)可以手术切除,但由于其他原因(如高龄、严重肝硬化等)不能或不愿接受手术的Ib期和IIa期病人;(3)多发结节型肝癌;(4)门静脉主干未完全阻塞,或虽完全阻塞但肝动脉与门静脉间代偿性侧支血管形成;(5)肝肿瘤破裂出血或肝动脉-门脉静分流造成门静脉高压出血;(6)控制局部疼痛、出血以及栓堵动静脉瘘;(7)肝癌切除术后,DSA造影可以早期发现残癌或复发灶,并给予介入治疗。3.禁忌证:(1)肝功能严重障碍(Child-Pugh C级),包括黄疸、肝性脑病、难治性腹水或肝肾综合征;(2)凝血功能严重减退,且无法纠正;(3)门静脉主干完全被癌栓栓塞,且侧支血管形成少;(4)合并活动性肝炎或严重感染且不能同时治疗者;(5)肿瘤远处广泛转移,估计生存期<3个月者;(6)恶液质或多器官功能衰竭者;(7)肿瘤占全肝比例≥70%癌灶(如果肝功能基本正常,可考虑采用少量碘油乳剂分次栓塞);(8)外周血白细胞和血小板显著减少,白细胞<3.0×109/L(非绝对禁忌,如脾功能亢进者,与化疗性白细胞减少有所不同),血小板<50×109/L;(9)肾功能障碍:肌酐>2mg/dl或者肌酐清除率<30ml/min。4. 操作程序要点和分类90(证据等级3):(1)肝动脉造影,通常采用Seldinger方法,经皮穿刺股动脉插管,导管置于腹腔干或肝总动脉行DSA造影,造影图像采集应包括动脉期、实质期及静脉期;应做肠系膜上动脉造影、注意寻找侧枝供血。仔细分析造影表现,明确肿瘤的部位、大小、数目以及供血动脉。(2)根据肝动脉插管化疗、栓塞操作的不同,通常分为:①肝动脉灌注化疗:经肿瘤供血动脉灌注化疗,常用化疗药物有蒽环类、铂类等。②肝动脉栓塞:单纯用栓塞剂堵塞肝肿瘤的供血动脉。③肝动脉化疗栓塞:把化疗药物与栓塞剂混合在一起,经肿瘤的供血动脉支注入。TACE治疗最常用的栓塞剂就是碘油乳剂、标准化明胶海绵颗粒,还有药物洗脱微球。先灌注一部分化疗药物,一般灌注时间不应<20 min。然后将另一部分化疗药物与碘油混合成乳剂进行栓塞。碘油用量一般为5-20 ml,不超过30 ml。在透视监视下依据肿瘤区碘油沉积是否浓密、瘤周是否已出现门静脉小分支影为界限。在碘油乳剂栓塞后加用颗粒性栓塞剂(如:标准化明胶海绵颗粒、微球、聚乙烯醇颗粒等)。提倡使用超液化乙碘油与化疗药物充分混合成乳剂,尽量避免栓塞剂返流栓塞正常肝组织或进入非靶器官。栓塞时应尽量栓塞肿瘤的所有供养血管,以尽量使肿瘤去血管化。5. TACE术后常见不良反应:栓塞后综合症,是TACE治疗的最常见不良反应,主要表现为发热、疼痛、恶心和呕吐等。发热、疼痛的发生原因是肝动脉被栓塞后引起局部组织缺血、坏死,而恶心、呕吐主要与化疗药物有关。此外,还有穿刺部位出血、白细胞下降、一过性肝功能异常、肾功能损害以及排尿困难等其他常见不良反应。介入治疗术后的不良反应会持续5-7天,经对症治疗后大多数病人可以完全恢复。6 疗效评价:根据实体瘤mRECIST评价标准以及EASL评价标准评估肝癌疗效,长期疗效指标为病人总生存时间(Overall survival, OS);短期疗效:评价指标为肿瘤的影像学应答和手术至疾病进展时间(Time to progress,TTP)。7.影响TACE远期疗效的主要因素包括84:(1)肝硬化程度、肝功能状态;(2)血清AFP水平;(3)肿瘤的容积和负荷量;(4)肿瘤包膜是否完整;(5)门静脉有无癌栓;(6)肿瘤血供情况;(7)肿瘤的病理分型。8.随访及TACE间隔期间治疗:一般建议第一次TACE治疗后3-6周时复查CT和/或MRI、肿瘤相关标志物、肝肾功能和血常规检查等;若影像学检查显示肝脏的瘤灶内的碘油沉积浓密、瘤组织坏死并且无增大和无新病灶,暂时不做TACE治疗。至于后续TACE治疗的频率应依随访结果而定,主要包括病人对上一次治疗的反应、肝功能和体能状况的变化。随访时间可间隔1-3个月或更长时间,依据CT和/或MRI动态增强扫描评价肝脏肿瘤的存活情况,以决定是否需要再次进行TACE治疗。目前主张综合TACE治疗,即TACE联合其它治疗方法,目的是控制肿瘤、提高病人生活质量和让病人带瘤长期生存。9.TACE治疗时注意点:(1)提倡用微导管超选择性插管。插入肿瘤的供血动脉支,精准地注入碘油乳剂和颗粒性栓塞剂,提高疗效和保护肝功能。(2)可使用门静脉内支架置放术和碘-125粒子条或碘-125粒子门静脉支架置放术,有效处理门静脉主干癌栓91(证据等级2)。(3)TACE联合消融治疗:目前有两种TACE联合热消融治疗方式。①序贯消融:先行TACE治疗,术后1-4周内加用射频或微波消融。②同步消融:在TACE治疗时,同时给予射频或微波消融,可以明显提高临床疗效,并减轻肝功能损伤92(证据等级2)。(4)颗粒性栓塞剂的应用:包括标准化明胶海绵颗粒、聚乙烯醇颗粒、微球、药物洗脱微球等。常规TACE常使用标准化明胶海绵微粒与碘油联合。药物性洗脱微球(Drug-eluting beads,DEB)是一种新的栓塞剂,可携带化疗药物。文献报道DEB在肿瘤客观有效率及总获益率方面具有优势。但是,近期文献报道结果显示两种方法治疗肝癌的疗效无显著性差异。(5)重视局部加局部治疗和局部联合全身治疗84:①TACE联合消融(RFA、MWA等)治疗91(证据等级2);②TACE联合放射治疗91(证据等级2):主要指门静脉主干癌栓、下腔静脉癌栓和局限性大肝癌介入治疗后的治疗;③TACE联合II期外科手术切除:大肝癌或巨块型肝癌在TACE治疗后缩小并获得手术机会时,推荐外科手术切除91(证据等级3);④TACE联合全身治疗:包括联合分子靶向药物三氧化二砷、放射免疫靶向药物、基因治疗、免疫治疗及全身化疗等。(五)放射治疗放射治疗(简称放疗)分为外放疗和内放疗。外放疗是利用放疗设备产生的射线(光子或粒子)从体外对肿瘤照射。内放疗是利用放射性核素,经机体管道或通过针道植入肿瘤内。1. 外放射治疗:(1)适应证:对伴有门静脉/下腔静脉癌栓或肝外转移的IIIa期、IIIb期肝癌病人,多属于姑息性放疗,有一部分病人肿瘤缩小或降期,可获得手术切除机会93-95(证据等级3)。肝外转移包括淋巴结转移、肺转移、骨转移、肾上腺转移、脑转移、腹膜和胸腔内膜转移等,也可用于等待肝癌肝移植前的治疗。对肝外转移的病人,外放疗可减轻疼痛、梗阻或出血等症状,使肿瘤发展减缓,从而延长生存期96-98(证据等级3)。中央型肝癌切缘距肿瘤≤1cm的窄切缘术后可以辅助放疗99(证据等级3)。(2)照射靶区:大体肿瘤体积(Gross Tumor Volume,GTV)在增强CT中定义,必要时也需要参考MRI影像。肝癌出现淋巴引流区转移较少见,因此,临床靶体积(Clinical Target Volume,CTV)不包括淋巴引流区。对于已经出现淋巴结转移的病人,必须包括其下一站的淋巴引流区,作为CTV。其余情况(如局限于肝内、癌栓、肾上腺、肺转移等)的CTV为影像学可见的病灶外扩2到4 mm100。肿瘤移动度可以通过透视评估,但4D模拟CT技术更为准确。在常规放疗技术情况下,计划靶体积(Planning Target Volume,PTV)一般在CTV基础上外放5-15 mm。肝内靶区的勾划必须有动脉相、静脉相互相参考;MRI对肝内病灶较清楚,PET/CT可以了解肝外病灶情况,靶区的确定尽量多种影像学资料互相参考。肝癌放疗野设计的一个重要原则是充分利用正常肝组织所具有的强大再生能力,在设计放射野时,尤其是大肝癌,最好能保留一部分正常肝组织不受照射,从而使部分正常肝组织能得到再生。(3)照射剂量和正常组织耐受剂量:立体定向放疗时,肝功能为Child-Pugh A级,正常肝体积超过700 ml,<15 Gy×3次,正常肝>800 ml,<18 Gy×3次是安全剂量;一般推荐放疗剂量≥30-60 Gy/3-6次101。对姑息性放疗的肝癌病人,肿瘤的放疗剂量基本上取决于全肝和/或周围胃肠道的耐受量,大部分的报道以 40-70Gy常规分割剂量。正常组织耐受剂量:肝功能为Child-Pugh A者,常规分割放疗时,全肝的耐受量为28-30 Gy102,或非常规低分割放疗(每次分割剂量4-8 Gy)全肝的耐受量为23 Gy103。肝功能为Child-Pugh B者,肝脏对射线的耐受量明显下降。由于亚洲HCC病人常伴有肝硬化和脾功能亢进,导致胃肠道瘀血和凝血功能差,胃肠道的放射耐受剂量低于RTOG推荐的剂量104。(4)放疗技术:建议应用三维适形放疗(3-D Conformal radiotherapy,CRT))、调强放疗(Intensity modulated radiation therapy ,IMRT)、图像引导放疗(Image guided radiation therapy,IGRT)或立体定向放疗(Stereotactic body radiation therapy,SBRT)。图像引导下的调强放射治疗技术优于三维适形放疗105,螺旋断层放疗设备作为图像引导下的调强放疗,适合多发病灶的肝癌病人。肝癌的立体定向放射治疗必须满足以下条件:有四维CT的影像设备引导或肿瘤追踪系统,非常精确的病人体位固定,放射治疗前的个体化图像校正,放射治疗设备能聚焦到肿瘤以及肿瘤之外的射线梯度下降快。目前缺乏较高级别的临床资料支持质子放疗在肝癌病人的生存率优于光子。呼吸运动是导致肝脏肿瘤在放疗过程中运动和形变的主要原因。目前可采取多种技术以减少呼吸运动带来的影响,如门控技术、实时追踪技术和呼吸控制技术,根据四维CT确定内靶区(Internal target volume,ITV)等等。腹部加压简单易行,减少肝脏的呼吸动度,压腹部位在剑突与脐连线上半部,可最大程度减小肝脏呼吸动度106。2. 内放射治疗:放射性粒子植入是局部治疗肝癌的一种有效方法,包括90Y微球疗法107、131I单克隆抗体108、放射性碘化油109、125I粒子植入等,放射性粒子可持续产生低能X射线、γ射线或β射线,在肿瘤组织内或在受肿瘤侵犯的管腔(门静脉、下腔静脉或胆道)内植入放射性粒子后,通过持续低剂量辐射,最大程度杀伤肿瘤细胞。粒子植入技术包括组织间植入、门静脉植入、下腔静脉植入和胆道内植入,分别治疗肝内病灶、门静脉癌栓、下腔静脉癌栓和胆管内癌或癌栓。(六)全身治疗对于没有禁忌证的晚期肝癌病人,全身治疗可以减轻肿瘤负荷,改善肿瘤相关症状,提高生活质量,延长生存时间。1.抗肿瘤治疗及其疗效评价(1)分子靶向药物:迄今为止,索拉非尼仍然是唯一获得批准治疗晚期肝癌的分子靶向药物。两项大型国际多中心III期临床试验均充分证明了索拉非尼对于不同国家地区、不同肝病背景的晚期肝癌都具有一定的生存获益110(证据等级1)。常规推荐用法为400mg,po.,bid,应用时需注意对肝功能的影响。最常见的不良反应为腹泻、体重下降、手足综合征、皮疹、心肌缺血以及高血压等(证据等级1),一般发生在治疗开始后的2-6周内,可用于肝功能Child A、B级的病人(证据等级1)。而相对于肝功能Child B级,ChildA级的病人生存获益更明显111。(2)系统化疗:传统的细胞毒性药物,包括阿霉素、表阿霉素、氟尿嘧啶、顺铂和丝裂霉素等,在肝癌中的单药或传统联合用药有效率均不高,且毒副作用大,可重复性差。一个主要原因为化疗药物不但会激活乙肝病毒复制,还会损害病人的肝功能,加重肝炎肝硬化,导致化疗无法带来生存效益。根据EACH研究后期随访的数据,含奥沙利铂的FOLFOX4方案在整体反应率、疾病控制率、无进展生存期、总生存期方面,均优于传统化疗药物阿霉素,且耐受性和安全性较好112(证据等级2)。因此,奥沙利铂在我国被批准用于治疗不适合手术切除或局部治疗的局部晚期和转移性肝癌。化疗适应证主要为:①合并有肝外转移的晚期病人;②虽为局部病变,但不适合手术治疗和TACE者,如肝脏弥漫性病变或肝血管变异;③合并门静脉主干或下腔静脉瘤栓者;④多次TACE后肝血管阻塞和/或TACE治疗后复发的病人。化疗禁忌证为:①ECOG PS评分>2,Child-Pugh评分>7分;②白细胞计数<3.0 X 109/L或中性粒细胞计数<l.5×109/L,血小板计数<60×109/L,血红蛋白<90g/L;③肝、肾功能明显异常,氨基转移酶(AST或ALT)>5倍正常值和/或胆红素显著升高>2倍正常值,血清白蛋白<28g/L,肌酐(Cr)≥正常值上限,肌酐清除率(CCr)<50ml/min;④具有感染发热、出血倾向、中-大量腹腔积液和肝性脑病。其他药物:三氧化二砷治疗中晚期原发性肝癌具有一定的姑息治疗作用113(证据等级3)。在临床应用时,应注意监测肝肾毒性。(3)免疫治疗:肝癌免疫治疗主要包括免疫调节剂(干扰素α、胸腺肽α1(胸腺法新)等)65,114、免疫检查点阻断剂(CTLA-4阻断剂、PD-1/PD-L1阻断剂等)、肿瘤疫苗(树突细胞疫苗等)、细胞免疫治疗(细胞因子诱导的杀伤细胞,即CIK)113,115。这些治疗手段均有一定的抗肿瘤作用,但尚待大规模的临床研究加以验证。(4)中医药:中医中药治疗能够改善症状,提高机体的抵抗力,减轻放化疗不良反应,提高生活质量。除了采用传统的辨证论治、服用汤剂之外,我国药监部门业已批准了若干种现代中药制剂如槐耳颗粒、康莱特、华蟾素、榄香烯、肝复乐等用于治疗肝癌116,117,具有一定的疗效,病人的依从性、安全性和耐受性均较好(证据等级4)。但是,这些药物尚缺乏高级别的循证医学证据加以充分支持。(5)全身治疗的疗效评估:对于化疗病人,仍然采用Recist 1.1标准,可同时参考血清学肿瘤标记(AFP)以及肿瘤坏死程度的变化,一般在治疗期间每6-8周进行影像学评估,同时通过动态观察病人的症状、体征、治疗相关不良反应进行综合评估。鉴于索拉非尼、TACE治疗很少能改变肿瘤大小,故建议采用以肿瘤血管生成和密度改变为基础的疗效评估标准(mRecist标准)118,119。对于免疫治疗的评价,可参照irRC (immune-related response criteria)标准120,121。2.抗病毒治疗及其他保肝治疗:合并有乙肝病毒感染且复制活跃的肝癌病人,口服核苷(酸)类似物抗病毒治疗非常重要。宜选择强效低耐药的药物如恩替卡韦、替比夫定或替诺福韦脂等。TACE治疗可能引起乙型肝炎病毒复制活跃,目前推荐在治疗前即开始应用抗病毒药物。抗病毒治疗还可以降低术后复发率69,70(证据等级1)。因此,抗病毒治疗应贯穿肝癌治疗的全过程。肝癌病人在自然病程中或者治疗过程中可能会伴随肝功能异常,因此应及时适当的应用保肝药物,如异甘草酸镁注射液(甘草酸二铵肠溶胶囊)、复方甘草酸苷、还原型谷胱甘肽、多磷脂酰胆碱等;抗炎治疗药物如广谱水解酶抑制剂乌司他丁等;利胆类药物如腺苷蛋氨酸、熊去氧胆酸等。这些药物可以保护肝功能、提高治疗安全性、降低并发症、改善生活质量。3.对症支持治疗:适度的康复运动可以增强机体的免疫功能。另外,应加强对症支持治疗,包括在晚期肝癌病人中的积极镇痛、纠正贫血、纠正低白蛋白血症、加强营养支持,控制合并糖尿病病人的血糖,处理腹水、黄疸、肝性脑病、消化道出血等伴随症状。对于晚期肝癌病人,应理解病人者及家属的心态,采取积极的措施调整其相应的状态,把消极心理转化为积极心理,通过舒缓疗护让其享有安全感、舒适感而减少抑郁与焦虑。
丁振斌 主任医师 上海中山医院 肝肿瘤外科4016人已读 - 精选 原发性肝癌规范化诊治的专家共识
一、前 言原发性肝癌(PLC,以下简称肝癌)是临床上最常见的恶性肿瘤之一,全球发病率逐年增长,已超过62.6万/年, 居于恶性肿瘤的第5位; 死亡接近60万/年,位居肿瘤相关死亡的第3位。PLC在我国高发,目前,我国发病人数约占全球的55%;在肿瘤相关死亡中仅次于肺癌,位居第二。因此,肝癌严重威胁我国人民健康和生命。为了推动我国临床肿瘤学事业的发展,提高PLC多学科规范化综合治疗和研究水平,积极学习和应用国内、外的符合循证医学原则的高级别证据,制订符合我国国情的PLC临床实践指南,中国抗癌协会肝癌专业委员会(CSLC)、临床肿瘤学协作专业委员会(CSCO)和中华医学会肝病学分会肝癌学组共同发起,组织多学科专家参与,制定了本“原发性肝癌规范化诊治专家共识”。2007年11月10日、2008年4月5日和8月30日,先后在上海召开了三次专家共识研讨会。会议由叶胜龙和秦叔逵教授共同主持,吴孟超、汤钊猷、孙燕院士和管忠震教授亲临指导,国内有关PLC诊治领域的60多位著名专家出席会议。在会上,系统地复习了当前PLC的国际指南与共识,讨论了PLC的诊断、手术治疗(肝切除与肝移植)、介入治疗、局部消融治疗(主要包括射频消融、微波消融和高强度聚焦超声治疗)、放射治疗、生物治疗、分子靶向治疗、系统化疗以及中医药治疗等一系列问题。各位专家认真准备、积极参与,基于尊重循证医学证据的原则,与国际上的诊断治疗理念接轨,特别是针对我国PLC诊治的现状和发展,大家各抒己见、集思广益,提出了许多良好的建议。会后,由部分专家执笔,广泛征求意见,反复多次修改,最终形成了本共识。二、对国际肝细胞癌诊疗指南与共识的评价由于PLC中大多数是肝细胞癌(HCC),临床处理涉及内科、外科、介入、放疗、中医科和医学影像学等诸多学科,因此,对于肝癌的规范化诊断治疗需要多学科专家共同讨论制定,以便为患者在确诊后选择最适合的首选治疗和综合治疗措施。目前国际上已有可供借鉴参考的肝癌治疗指南,主要包括:①美国国家综合癌症网(NCCN)的肝癌临床实践指南;②美国肝病研究协会(AASLD)HCC临床治疗指南;③英国胃肠病学会(BSG)治疗指南;④美国外科学院(ACS)制定的共识;内容涉及到肝癌的分期、监测、筛查、诊断及治疗。(一)肝细胞癌的分期对于HCC的分期,在AASLD、ACS和NCCN指南中并不统一,侧重点也不尽相同。其中,NCCN采用的TNM分期方式在国际上是最为规范的,但被认可程度却比较低,原因在于:①对于HCC的治疗和预后至关重要的血管侵犯,在治疗前(特别是手术前)难以准确判断;②治疗HCC非常强调肝功能代偿,而TNM分期并没有说明患者的肝功能状况;③ 各版TNM分期的变化较大,难以比较评价。AASLD采用的是巴塞罗那肝癌中心(BCLC)分期与治疗策略,比较全面地考虑了肿瘤、肝功能和全身情况,并且具有循证医学高级别证据的支持,目前在全球范围比较公认而广泛采用。(二)肝细胞癌的监测和筛查上述四项国际指南都十分强调HCC的早期筛查和早期监测,均以循证医学证据作为依据,可信度较高。对于筛查指标的看法比较一致,主要包括血清甲胎蛋白(AFP)和肝脏超声检查两项。对于≥35岁的男性,具有HBV和(或)HCV感染,嗜酒的高危人群,一般是每隔6个月进行一次检查。对AFP> 400 μg/L而超声检查未发现肝脏占位者,应注意排除妊娠、活动性肝病以及生殖腺胚胎源性肿瘤;如能排除,应作CT和(或)MRI等检查。如AFP升高但未达到诊断水平,除了应该排除上述可能引起AFP增高的情况外,还应密切追踪AFP的动态变化,将超声检查间隔缩短至1~2个月,需要时进行CT和(或)MRI检查。若高度怀疑肝癌,建议做DSA肝动脉碘油造影检查。(三)肝细胞癌的诊断HCC诊断标准包括病理学诊断标准和临床诊断标准。诊断方法包括血清肿瘤标志物(AFP)检测、影像学检查(包括超声显像、CT、MRI和DSA血管造影等)以及病理组织学检查(主要是肝组织活检)。BSG指南提出,对于有肝硬化的患者,首先确定肝硬化的存在,随后以占位大小2 cm为界限开始诊断流程;而对于非肝硬化患者,则以AFP水平来引导诊断流程。在国际上应用AASLD的诊断流程较多,以占位<1 cm,1~2 cm和>2 cm,对肿物和诊断流程进行区分,着重强调早期诊断。(四)肝细胞癌的治疗ACS的共识指出HCC的治疗目标包括:治愈;局部控制肿瘤,为移植做准备;局部控制肿瘤,开展姑息治疗。提高生活质量也是重要的治疗目标之一。治疗方法大致包括手术(肝切除术、肝移植和姑息治疗手术)、非手术治疗(局部治疗、动脉化学栓塞、化疗、放疗、生物治疗以及分子靶向治疗)以及其他治疗方法(包括参加临床研究)。NCCN强调,在遵循循证医学的基础上与时俱进,其2008年版已引入了近两年来肝癌治疗领域的突破性进展,即将分子靶向治疗药物索拉非尼列为不能手术和晚期HCC患者的标准治疗选择之一。三、原发性肝癌的诊断(一)早期诊断早期诊断至关重要,从20世纪70~80年代起,由于血清AFP、实时超声显像和CT的逐步普及和广泛应用,大大促进了PLC的早期诊断。由于早期诊断率明显提高,手术切除率随之提高,预后亦获得明显改善;故PLC的诊断,尤其是早期诊断,是临床诊疗和预后的关键。就早期诊断而言,对于患者的肝病背景应予充分重视。我国95%的PLC患者具有乙肝病毒(HBV)感染的背景,10%有丙肝病毒(HCV)感染背景,还有部分患者HBV和HCV重叠感染。对下列危险人群应特别加以关注:中老年男性中HBV载量高者、HCV感染者、HBV和HCV重叠感染者、嗜酒者、合并糖尿病者以及有肝癌家族史者。此类人群在35~40岁后,每6个月应定期进行筛查(包括血清AFP检测和肝脏超声检查);当出现AFP升高或肝区“占位性病变”时,应立即进入诊断流程,严密观察,力争早期作出诊断。(二)肝癌的实验室诊断方法目前,在我国肝癌的定性诊断仍以检测血清AFP为主,应高度重视:(1)在我国,60%以上肝癌病例的血清AFP>400μg /L;(2)目前还没有其他肿瘤标志物的特异性可与AFP相媲美;(3)AFP检测较少依赖影像学设备和新技术。(三)肝癌的影像学诊断方法近年来,医学影像学检查手段的进步明显,为临床上PLC的"四定" (定位、定性、定量和定期)和制定治疗方案提供了可靠的依据。(1)超声检查:超声检查为非侵入性检查,对人体组织无任何不良影响,其操作简单、直观准确、费用低廉,方便无创,广泛普及,可用于肝癌的普查和治疗后随访。实时超声造影对于直径<3 cm的肝癌鉴别诊断具有重要的临床价值,常用于肝癌的早期发现和诊断,用于肝癌与肝囊肿和肝血管瘤的鉴别诊断较有参考价值,而术中超声直接在开腹后的肝脏表面探查,避免了超声衰减和腹壁、肋骨的干扰,可发现术前CT、超声检查皆未发现的肝内病灶。但是,超声检查容易受到检查者经验、手法和细致程度的限制。(2)多层螺旋CT:CT的分辩率远远高于超声,图像清晰而稳定,能全面客观地反映肝癌的特性,用于肝癌常规诊断检查和治疗后的随访检查。CT检查可清楚地显示肝癌的大小、数目、形态、部位、边界、肿瘤血供丰富程度,以及与肝内管道的关系;对门静脉、肝静脉和下腔静脉是否有癌栓,肝门和腹腔淋巴结是否有转移,肝癌是否侵犯邻近组织器官都有重要的诊断价值;还可通过显示肝脏的外形、脾脏的大小以及有无腹水来判断肝硬化的轻重,因此CT已经成为肝癌诊断重要的常规手段。特别是薄层、增强扫描有助于进一步明确肝癌的部位、范围、有无肝内转移和远处转移,可以显著提高小肝癌的检出率;肝动脉碘油造影3~4周后进行CT扫描也能有效发现小肝癌病灶。(3)磁共振成像(MRI),具有很高的组织分辨率、多参数、多方位成像等特点,是继CT之后的又一有效而无创伤性的肝癌检查诊断方法,有助于肝癌的鉴别诊断。应用肝脏特异性MRI造影剂能够提高肝脏转移病灶和小肝癌检出率,对肝癌与肝脏局灶性增生结节、肝腺瘤等的鉴别亦有较大帮助;另外,对于PLC患者TACE治疗后的疗效的跟踪观察,MRI可能较CT有更高的临床价值。MRI对肝内小病灶的检出、血管的情况以及肿瘤内结构的显示有独到之处,可以作为CT检查的补充。(4)正电子发射计算机断层成像-CT(PET-CT)是将PET与CT融为一体而成的功能分子影像成像系统,既可由PET功能显像反映肝脏占位详尽的功能与代谢等分子信息(生化代谢情况),又可通过CT形态显像进行病灶的精确解剖定位,并且同时全身扫描可以了解整体状况和评估转移情况,达到早期发现病灶和诊断疾病的目的,具有灵敏准确、分辩率高、直观性好等特点,在肝癌诊断中具有一定的作用;另外,对于放疗中生物靶区的定位以及适形调强放疗计划的实施也具有重要价值。(5)选择性肝动脉造影是侵入性检查,碘油造影同时还具有治疗作用,可以明确显示肝脏小病灶及其血供情况,适用于其他检查后仍未能确诊时。(四)肝癌的病理诊断病理学检查是诊断原发性肝癌的金标准,但仍需特别重视结合临床。肝癌病理组织学主要分为肝细胞癌(HCC)、肝内胆管癌(Intrahepatic cholangiocarcinoma, ICC)和混合性肝癌三种类型。纤维板层癌是HCC的一种特殊类型,常见于青少年,多不伴肝硬化,生长缓慢;预后较好。鉴于肝细胞癌与肝内胆管癌在发病机制、生物学特性、临床表现、治疗方法和预后等方面有所不同,应注意鉴别,分别制定相应的诊疗规范。主要诊断依据如下:(1) HCC以梁索状排列多见,癌细胞呈多边形,细胞质嗜酸性,细胞核圆形,梁索间衬覆血窦,但也可出现多种细胞学和组织学上的特殊类型,如常见的假腺管结构等,需要仔细鉴别诊断。代表性免疫组化染色:肝细胞抗原(Hep Par1)示细胞质阳性,多克隆性癌胚抗原(pCEA)示细胞膜(毛细胆管)阳性,CD34示微血管弥漫阳性。(2) HCC的大体分型,可以参考中国肝癌病理研究协作组于1979年制定的“五大型六亚型”分类,癌细胞分化程度可参考Edmondson-Steiner四级分级法。(3) ICC以腺管状排列为主,癌细胞呈立方形或低柱状,细胞质淡染或嗜碱性,纤维间质丰富,但也可出现多种细胞学和组织学上的特殊类型,需要仔细鉴别诊断。代表性免疫组化染色:细胞角蛋白19(CK19)和粘糖蛋白-1(MUC-1)示细胞质阳性。(4)ICC的大体类型可分为结节型、管周浸润型和结节浸润型,癌细胞分化程度可分为好、中、差。(5) 混合性肝癌为在一个肝癌结节内同时存在肝细胞癌和胆管癌两种成分,生物学特性介于两种类型之间。小肝癌不完全等于早期肝癌的概念。有些小肝癌早期就可以出现微小转移灶,其手术切除治疗的效果不一定很好;另外,早期肝癌也并不完全代表肝功能处于代偿状态,也不代表都是可切除的。病理诊断报告的内容应包括:肿瘤的部位、大小、数目、细胞和组织学类型、分化程度、血管和包膜侵犯、卫星灶和转移灶,以及癌旁肝组织病变情况等。病理诊断报告中还可附有与肝癌药物靶向分子、生物学行为以及判断预后相关的免疫组化和分子标志物的检测结果,以供临床参考。四、原发性肝癌的外科治疗PLC的外科治疗包括肝切除术和肝移植术。肝切除术的基本原则包括:①彻底性:完整切除肿瘤、切缘无残留肿瘤;②安全性:最大限度保留正常肝组织,降低手术死亡率及手术并发症。在术前应对肝功能储备进行评价,通常采用Child-Pugh分级评价肝实质功能,采用CT和(或)MRI计算余肝体积。(一)肝切除术1. 肝切除的方法分类肝切除方法包括根治性切除和姑息性切除。根治性切除是指:①肿瘤数目不超过2个;②无门脉主干及一级分支、总肝管及一级分支、肝静脉主干及下腔静脉癌栓;③无肝内、外转移;完整切除肉眼所见肿瘤,切缘无残癌;④术后影像学检查未见肿瘤残存,术前AFP阳性者术后随访2个月内血清AFP降至正常。2. 原发性肝癌手术治疗的适应证随着现代肝脏外科手术技术的进步,肿瘤大小并不是手术的关键限制因素。能否切除和切除的疗效不仅与肿瘤大小和数目有关,还与肝脏功能、肝硬化程度、肿瘤部位、肿瘤界限、有无完整包膜及静脉癌栓等有非常密切的关系。3. 中华外科学会肝脏学组颁布的肝癌手术适应证(1)患者的一般情况(必备条件):一般情况良好,无明显心、肺、肾等重要脏器器质性病变;肝功能正常、或仅有轻度损害(Child-Pugh A级);或肝功能分级属B级,经短期护肝治疗后恢复到A级;肝储备功能(如ICGR15)基本在正常范围以内;无不可切除的肝外转移性肿瘤。(2)可行根治性肝切除的局部病变须满足下列条件:①单发肝癌,表面较光滑,周围界限较清楚或有假包膜形成,受肿瘤破坏的肝组织<30%,或受肿瘤破坏的肝组织>30%,但无瘤侧肝脏明显代偿性增大,达全肝组织的50%以上;②多发性肿瘤,结节<3 个,且局限在肝脏的一段或一叶内。(3)可行姑息性肝切除的局部病变须符合下列条件:①3~5个多发性肿瘤,超越半肝范围者,行多处局限性切除;②肿瘤局限于相邻2~3个肝段或半肝内,无瘤肝组织明显代偿性增大达全肝的50%以上;③肝中央区(中叶或Ⅳ、Ⅴ、Ⅷ段)肝癌,无瘤肝组织明显代偿性增大达全肝的50%以上;④肝门部有淋巴结转移者,肿瘤切除同时行淋巴结清扫或术后治疗;⑤周围脏器受侵犯者一并同时切除。(4)姑息性肝切除还涉及以下几种情况:原发性肝癌合并门静脉癌栓(PVTT)和(或)腔静脉癌栓、肝癌合并胆管癌栓、原发性肝癌合并肝硬化门脉高压、难切性肝癌的切除。每种情况均有其对应手术治疗适应证(表1)。此外,对于不适宜姑息性切除的肝癌,应考虑姑息性非切除外科治疗,如术中肝动脉结扎和(或)肝动脉、门静脉插管化疗等。表1原发性肝癌姑息性肝切除适应证原发性肝癌病变情况姑息性肝切除适应证原发性肝癌合并门静脉癌栓(PVTT)和(或)腔静脉癌栓▲门静脉主干切开取癌栓术,同时作姑息性肝切除▲按原发性肝癌肝切除手术适应证的标准判断,肿瘤是可切除的▲癌栓充满门静脉主支或/和主干,进一步发展,很快将危及患者生命▲估计癌栓形成的时间较短,尚未发生机化▲如作半肝切除,可开放门静脉残端取癌栓▲如癌栓位于肝段以上小的门静脉分支内,可在切除肝肿瘤的同时连同该段门静脉分支一并切除▲如术中发现肿瘤不可切除,可在门静脉主干切开取癌栓术后,术中作选择性肝动脉插管栓塞化疗或门静脉插管化疗、冷冻或射频治疗等▲合并腔静脉癌栓时,可在全肝血流阻断下,切开腔静脉取癌栓,并同时切除肝肿瘤原发性肝癌合并胆管癌栓患者一般情况:▲基本要求同肝切除术▲这种患者有阻塞性黄疸,不能完全按Child-Pugh分级判断肝功能,应强调患者全身情况、A/G比值和凝血酶原时间等局部病变情况:▲ 胆总管切开取癌栓术,同时作姑息性肝切除▲ 按原发性肝癌肝切除手术适应证的标准判断,肿瘤是可切除的▲ 癌栓位于左肝管或右肝管、肝总管、胆总管▲癌栓未侵及健侧二级以上胆管分支▲估计癌栓形成的时间较短,尚未发生机化▲如癌栓位于肝段以上小的肝管分支内,可在切除肝肿瘤的同时连同该段肝管分支一并切除▲如术中发现肿瘤不可切除,可在切开胆总管取癌栓术后,术中作选择性肝动脉插管栓塞化疗、冷冻治疗或射频治疗等原发性肝癌合并肝硬化门静脉高压症可切除的肝癌▲有明显脾肿大、脾功能亢进表现者,可同时作脾切除术▲有明显食道胃底静脉曲张,特别是发生过食道胃底曲张静脉破裂大出血者,可考虑同时作贲门周围血管离断术▲有严重胃粘膜病变者,可考虑作脾肾分流术或其他类型的选择性门腔分流术不可切除的肝癌▲有明显脾肿大、脾功能亢进表现,无明显食道胃底静脉曲张者,作脾切除的同时,在术中作选择性肝动脉栓塞化疗、冷冻治疗或射频治疗等▲有明显食道胃底静脉曲张,特别是发生过食道胃底静脉破裂大出血,无严重胃粘膜病变,可作脾切除,或脾动脉结扎加冠状静脉缝扎术;是否作断流术,根据患者术中所见决定。肝癌可术中作射频或冷冻治疗,不宜作肝动脉插管栓塞化疗对于肝内微小病灶的治疗值得关注。部分微小病灶经影像学检查或术中探查都不能发现,致使肝切除后的复发率升高。如果怀疑切除不彻底,那么术后采用TACE是理想的选择,因除了治疗的意义外,还有检查残留癌灶的意义。如有残留癌灶,应及时作出补救措施。此外,术后病例应作肝炎病毒载量 (HBV DNA/HCV RNA) 检查;如有指征,应进行抗病毒治疗,以减少肝癌再发的可能。(二)肝移植术1. 肝移植选择标准:目前,我国每年大约开展4,000例的肝移植手术,其中肝癌患者高达40%。在我国,肝癌肝移植仅作为补充治疗,用于无法手术切除的,不能进行射频、微波和TACE治疗的,肝功能不能耐受的患者。关于肝移植适应证,国际上主要广泛采用Milan标准和UCSF标准;而国内尚无统一标准,已有多家单位提出了不同标准,主要的有上海复旦标准、杭州标准及成都标准等,对于无大血管侵犯、淋巴结转移及肝外转移的要求比较一致,但对肿瘤的大小和数目的要求不尽相同。我国的标准扩大了肝癌肝移植的适应证范围,能使更多的肝癌患者因手术受益,可能更为符合我国国情和患者的实际。但有待于依据高水平的循证医学证据而形成相对统一的中国标准。2. 肝移植术后复发的预防:一般认为术后进行适当的化疗及抗病毒治疗有可能减少肝癌复发、改善生存,但需要进一步研究。3. 肝移植及肝切除的选择:外科治疗手段主要是肝切除和肝移植,如何选择,目前尚无统一的标准。一般认为:对于局限性肝癌,如果患者不伴有肝硬化,则应首选肝切除;如果合并肝硬化,肝功能失代偿(Child-Pugh C级),且符合移植条件,应首选肝移植。对于可切除的局限性肝癌且肝功能代偿良好(Child-Pugh A级),是否可进行肝移植,目前争议比较大。欧洲专家支持首选肝移植,理由是肝切除的复发率高,符合Milan标准的肝移植患者的长期生存率和无瘤生存率显著优于肝切除的患者。就某一患者而言,强调根据具体情况,综合评价分析,制定手术方式。此外,对于可切除的肝癌,即使影像学表现为局限性可切除肝癌,也应进行术前血管造影,因其可发现其他影像学手段无法发现的病灶,还可明确有无血管侵犯。五、原发性肝癌的介入治疗(一)适用人群1. 不能手术切除的中晚期原发性肝癌患者;2. 能手术切除,但由于其他原因(例如高龄、严重肝硬化等)不能或不愿进行手术的患者。对于上述患者,放射介入治疗可以作为非手术治疗中的首选方法。国内临床经验表明,放射介入治疗对于包膜比较完整的巨块型肝癌、大肝癌比较有效。对于可切除肝癌,优先选择外科切除或介入治疗的影响因素包括:①血清AFP水平;②肿瘤病灶是否包膜完整、边界清楚;③门静脉有无癌栓。(二)适应证和禁忌证肝动脉化疗(HAI)和肝动脉栓塞(HAE)均有明确的适应证和禁忌证(表2);化疗性栓塞(TACE)非常重要,单纯给予HAI是不够的。表2肝动脉化疗(HAI)和肝动脉栓塞(HAE)的适应证和禁忌证适应证禁忌证肝动脉化疗▲失去手术机会的原发或继发性肝癌▲肝功能较差或难以超选择性插管者▲肝癌手术后复发或术后预防性肝动脉灌注化疗▲肝功能严重障碍者▲大量腹水者▲全身情况衰竭者▲白细胞和血小板显著减少者肝动脉栓塞▲肝肿瘤切除术前应用,可使肿瘤缩小,利于切除。同时能明确病灶数目,控制转移▲无肝肾功能严重障碍、无门静脉主干完全阻塞、肿瘤占据率小于70%▲外科手术失败或切除术后复发者▲控制疼痛,出血及动静脉瘘▲肝癌切除术后的预防性肝动脉化疗栓塞术▲肝癌肝移植术后复发者▲肝功能严重障碍,属Child-Pugh C级▲凝血机能严重减退,且无法纠正▲门静脉高压伴逆向血流以及门脉主干完全阻塞,侧支血管形成少者(若肝功基本正常可采用超选择导管技术对肿瘤靶血管进行分次栓塞)▲感染,如肝脓肿▲全身已发生广泛转移,估计治疗不能延长患者生存期▲全身情况衰竭者▲癌肿占全肝70%或以上者(若肝功能基本正常可采用少量碘油分次栓塞)(三)操作程序和要点1. 肝动脉造影:采用Seldinger方法,经动脉穿刺插管,导管置于腹腔干或肝总动脉造影。造影图像采集应包括动脉期、实质期及静脉期;2. 灌注化疗:仔细分析造影表现,明确肿瘤的部位、大小、数目以及供血动脉后,超选择插管至肿瘤供血动脉内给予灌注化疗;3. 肝动脉栓塞:需选择合适的栓塞剂。一般用超液化乙碘油与化疗药物充分混合成乳剂。碘油用量应根据肿瘤的大小、血供情况、肿瘤供血动脉的多寡灵活掌握。栓塞时必须采用超选择插管。PLC的TACE非常强调超选择插管。过去仅对小肝癌强调超选择插管,现在特别强调针对所有的肝癌,除多发结节以外,均应采用超选择性插管。对于大肝癌,超选择插管更有利于控制肿瘤的生长,保护正常肝组织。(四)随访和治疗间隔随访期通常为介入治疗后35天至3个月,原则上为患者从介入术后恢复算起,至少持续3周以上。介入治疗的频率依随访结果而定:若介入术后一个月影像学检查肝肿瘤病灶内碘油沉积浓密,肿瘤组织坏死且无新病灶或无新进展,则暂不作介入治疗。治疗间隔应尽量延长。最初几次治疗时密度可加大,此后,在肿瘤不进展的情况下延长治疗间隔,以保证肝脏功能的恢复。在治疗间隔期,可利用MRI动态增强扫描评价肝脏肿瘤的存活情况,以决定是否需要再次进行介入治疗。(五)肝动脉化疗栓塞术(TACE)为主的“个体化”方案1. 肝癌缩小后二期切除:在大肝癌介入治疗明显缩小以后,可采取外科手术。2. 肝癌术后的预防性介入治疗:由于大部分PLC在肝硬化的基础上发生,多数病例为多发病灶。部分小病灶可能在术中未被发现。对于怀疑为非根治性切除的患者,建议术后40天左右做预防性灌注化疗栓塞。3. 门静脉癌栓及下腔静脉癌栓的治疗:可采用放置支架和放射治疗。关于下腔静脉癌栓,如果是肿瘤增大压迫引起,且患者无症状,可不放置支架,仅采用TACE,观察肿瘤能否缩小。如果癌栓是肿瘤侵犯下腔静脉引起,主张在TACE治疗的同时放置下腔静脉支架或先放置支架。4. TACE为主的个体化方案还涉及到肝肿瘤破裂出血的治疗、肝癌伴肺转移的治疗、TACE联合消融、放疗、基因和靶向治疗等方面。总之,应该强调积极采用以TACE为主的综合治疗措施,方能获得良好的疗效。六、原发性肝癌的消融治疗(一)概述消融治疗是指影像技术引导下在局部直接杀灭肿瘤的一类治疗手段,目前以射频和微波消融及无水酒精注射最为常用。消融的途径可经皮肤入路,也可在腹腔镜手术或开腹手术中应用。影像引导手段主要包括超声和CT。在超声引导下经皮消融的方法,具有微创安全、操作简便、易于反复施行、成本费用相对低廉的显著优点,对于有肝硬化背景和高度复发倾向的PLC患者来说,临床依从性较高,在我国已得到广泛的应用。关于肿瘤消融技术的规范应用,已取得国际共识(参见Radiology 2005; 235:728–739)。(二)适应证和禁忌证1. 适应证:对直径≤5 cm的单发肿瘤或最大直径≤3 cm的3个以内多发结节,无血管、胆管侵犯或远处转移,肝功能Child-Pugh A或B级的早期肝癌患者,射频或微波消融是外科手术以外的最好选择。对单发肿瘤直径≤3 cm的小肝癌多可获得根治性消融;酒精消融也可能达到同样的目的。无严重肝肾心脑等器官功能障碍、凝血功能正常或接近正常的肝癌,不愿意接受手术治疗的小肝癌以及深部或中心型小肝癌,手术切除后复发、中晚期癌等各种原因而不能手术切除的肝癌,肝脏转移性肿瘤化疗后、患者等待肝移植前控制肿瘤生长以及移植后复发转移等均可采取消融治疗。由于局部治疗有一定的局限,按照现有的技术水平不推荐对 >5cm 的病灶单纯施行消融治疗。肿瘤距肝门部肝总管、左右肝管的距离应至少为5mm。对多个病灶或更大的肿瘤,根据患者肝功能状况,采取治疗前肝动脉化疗栓塞(TACE或TAE)+射频联合治疗明显优于单纯的射频治疗;对位于肝表面、邻近心膈、胃肠管区域的肿瘤,可选择开腹或腹腔镜下治疗,也可以射频结合无水酒精注射;此外射频术后进行TACE或其他治疗也有可能提高疗效。2.禁忌证:(1)位于肝脏脏面,其中1/3以上外裸的肿瘤;(2)肝功能Child-Pugh C级,TNM Ⅳ期或肿瘤呈浸润状;(3)肝脏显著萎缩,肿瘤过大,需消融范围达1/3肝脏体积者;(4)近期有食管(胃底)静脉曲张破裂出血;(5)弥漫性肝癌,合并门脉主干~二级分支或肝静脉癌栓;(6)主要脏器严重的功能衰竭;(7)活动性感染尤胆系炎症等;(8)不可纠正的凝血功能障碍及血象严重异常血液病;(9)顽固性大量腹水;意识障碍或恶液质。(三)基本技术要求1. 强调应在影像技术引导下进行操作,以保证治疗的安全性、准确性和有效性。2. 消融范围应力求包括0.5 cm的癌旁组织,以获得“安全边缘”,彻底杀灭肿瘤。对边界不清晰、形状不规则浸润型癌或转移癌,在邻近肝组织及结构条件许可下建议扩大瘤周安全范围达1 cm或以上。3. 评估局部疗效的规范方法是消融后一个月左右,采用对比增强CT/MRI 或超声造影判定肿瘤是否被完全消融 (Complete response, CR)。获得CR的病灶表现为完全无血供即表现为无增强。若消融不完全,可即刻补充治疗。若经3次消融仍不能获得CR,应放弃消融疗法,改用其他治疗。4. 治疗后应定期随访复查,以及时发现可能的局部复发和肝内新病灶,利用经皮消融微创安全和简便易于反复施行的优点,有效地控制肿瘤进展。(四)常见消融手段的选择和应用1. 射频消融 (RFA):是应用广泛的热消融手段。大量文献以及几项随机对照的临床试验 (RCT)显示,与酒精消融比较,RFA对3~5 cm的肿瘤具有根治率高、所需治疗次数少和远期生存率高的显著优势。射频消融存在导致针道转移、穿刺所致周围脏器损伤及诱发肝癌破裂等问题,此外也不适用于位于影像盲区的肝癌。2. 微波消融 (MWA):也是常用的热消融方法。随机的和回顾性比较研究表明,MWA和RFA在局部疗效、并发症发生率以及远期生存方面都无显著差异。现在的MWA技术也能一次性灭活肿瘤。建立温度监控系统可以调控有效热场范围,保证凝固效果。血供丰富的肿瘤,先凝固阻断肿瘤主要滋养血管,再灭活肿瘤可以提高疗效。3. 无水酒精注射(PEI):适用于直径在3 cm以内的小肝癌及复发小肝癌的治疗。对3 cm以上不适合手术的肝癌或复发灶,也可起到姑息治疗的作用。临床上有10%~25%的病灶部位贴近肝门、胆囊、胃肠道等组织脏器,射频或微波等热消融治疗将可能造成损伤。对这些部位的肿瘤可以采用酒精注射或与热消融并用,以防止并发症发生。4. 高强度聚焦超声消融(high intensity focused ultrasound,HIFU):与其他消融方法相比,HIFU是一种非侵入性的体外适形治疗肿瘤的新技术,疗效确切。存在的问题:HIFU聚焦区域小,常需反复多次进行;通过超声探测肿瘤存在盲区;治疗中存在照射通道被肋骨遮挡的问题,甚至需要切除肋骨,违背微创的初衷;由于肝脏受呼吸运动的影响, 准确定位有一定的难度。目前认为,HIFU 还不能作为PLC单独治疗模式,可以考虑作为TACE后进行补充治疗,或作为姑息治疗手段。(五)消融治疗与外科手术治疗小肝癌的有关问题目前, 对于5 cm以下的肝癌是首选外科治疗还是经皮消融治疗,学术界存在争议。已有数项临床前瞻性随机对照和回顾性比较研究结果均显示局部消融(主要是射频和微波)治疗可获得与手术切除治疗小肝癌相近的远期生存疗效;但是两者相比,外科手术切除的优势是积累的经验丰富、普及率高和复发率低,而经皮局部消融并发症发生率低、恢复快、住院时间短。就治疗效果而言,有两项随机对照研究显示消融治疗和手术切除者的生存率没有明显差别,但在无瘤生存期(DFS)及复发率上,手术更具优势。在临床上,应该根据患者的肝功能和体质,肿瘤的大小、数目、位置,本单位技术力量以及患者的意愿等进行全面考虑,选择合适的初始治疗手段。一般认为,如果患者能耐受解剖性肝切除,应首选外科切除,因为可清除相应肝段或肝叶的微小转移灶,有效地防止术后复发。大多数专家认为:外科治疗仍是小肝癌治疗的首选,对于同时满足局部手术治疗和消融治疗指征的≤5 cm肝癌,在有条件时还是进行手术治疗,局部消融可作为手术切除之外的另一种治疗选择。对于肝脏深部或中央型≤3 cm的肝癌,局部消融可以达到手术切除疗效,获得微创下根治性消融,可优先选择;对于3~5 cm 的肝癌,通过选择适宜的仪器针具、掌握合理的消融技术、积累一定的治疗经验等,可提高治疗效果。此外肝移植也属于手术治疗范畴,目前还缺乏消融治疗与肝移植、解剖性肝切除术的比较数据。对于大肝癌(>5 cm),是否可以多位点或分次消融或开腹或腹腔镜下消融,目前缺乏循证医学证据资料可供参考,因此不宜推荐。射频消融与微波消融两者都是通过热效应使得肿瘤组织细胞坏死。微波消融导入的能量可能较大,消融的范围相对更大,不过两者之间无论是在局部疗效和并发症,还是生存率方面都无显著差异。消融治疗后应定期观察病灶坏死的情况,如有病灶残留,应积极治疗,提高消融治疗的疗效。七、原发性肝癌的放射治疗放射治疗是恶性肿瘤治疗的基本手段之一,但在20世纪90年代以前,由于放疗效果较差,且对肝脏损伤较大,因此原发性肝癌患者较少接受放疗。20世纪90年代中期之后,三维适形放疗(3-dimensional conformal radiation therapy, 3DCRT)和调强适形放疗(intensity modulated radiation therapy, IMRT)等现代放疗技术逐渐成熟,为放疗在肝癌治疗中的应用提供了新的机会。国内外学者已经陆续报道了采用3DCRT和IMRT技术治疗不能手术切除的原发性肝癌的研究;对于局限于肝内的肝癌患者,放疗结合介入治疗的3年生存率可达到25%~30%。(一)肝癌的放疗指征①肿瘤局限,因肝功能不佳不能进行手术切除,或肿瘤位于重要解剖结构,在技术上无法切除,或拒绝手术。要求一般情况好,如KPS≥70分。②手术后有残留病灶者。③需要肝脏局部肿瘤处理,否则会产生一些并发症,如肝门胆管的梗阻、门静脉和肝静脉的瘤栓,对肝门胆管的梗阻患者可以先进行引流,缓解黄疸,再进行放疗。④远处转移灶的治疗,如淋巴结转移、肾上腺转移以及骨转移,放疗可减轻患者的症状,改善生活质量。(二)肝癌放疗的技术1. 放疗剂量的分割:已有的临床经验表明,大分割照射,如每次5 Gy左右,每日1次,每周照射3次,总剂量50 Gy左右,对肿瘤的杀灭效应强,但是对正常肝脏的放射损伤也大。常规分割放射,如2Gy/次,每日1次,每周照射5次,总剂量50~62 Gy,正常肝脏的耐受性好,对肿瘤也有明显的抑制。如果采用4-8Gy/Fx的低分割适形放疗,一旦发生放射性肝损伤,70%以上的患者在短期内死于肝衰竭。然而,究竟哪种分割方法更好,还需进一步的临床研究来证明。2. 放射计划(1)放疗技术:剂量学比较的结果显示,与3DCRT比较,IMRT放疗的靶区剂量适形性更好,而且正常肝脏的受照剂量减小。因此一般先用3DCRT技术,如果达不到剂量学的要求,则用IMRT技术。IMRT更适用于下述患者:肝癌体积较大以致正常肝受到较大剂量照射时,或患者的肝硬化严重,不能耐受大剂量照射时。(2)呼吸的控制:建议使用呼吸控制技术,如主动呼吸控制调节器(active breath coordinator,ABC)以限制肿瘤在放疗中的运动,从而减少对正常肝脏的放射剂量。(3)靶区定位:为了提高肝癌大体肿瘤范围(GTV)勾画的准确性,建议CT采用动脉相,因为肝癌绝大多数属于动脉供血;但是在确定静脉癌栓时,必须采用静脉相,动脉相可作为参考,因为有些癌栓也有动脉血供。在MRI上勾画时,建议用T2相;同时建议使用CT和MRI图像的融合技术,以提高GTV勾画的精确性。因此,对于GTV,建议采用CT和MRI图像融合技术,并且结合TACE后的碘油沉积来确定。在实际工作中,确定肝癌的GTV时要留有充分的余地,因为许多患者的肿瘤在CT和MRI图像上的边界并不很清楚。临床肿瘤体积(CTV)为GTV外加4 mm;计划放疗靶区(PTV)在CTV的基础上再外扩5-10mm(根据不同医院的情况决定);所以,从GTV 到PTV,要外扩10-15mm。当然,如果使肝脏的放射剂量超过了耐受的范围,为了使放疗能够进行,可以考虑减少外扩的距离。计划体积(PTV)在使用ABC装置条件下为CTV外加6 mm。在没有使用ABC时更要根据患者的呼吸来确定。目前,有一些单位在放疗前先进行2个疗程的介入栓塞化疗(TACE),间隔3~6周后,再进行评估是否需要放射治疗。这种方案可能具有以下好处:①TACE过程中可以发现和治疗小的肝癌病灶;②有利于肿瘤靶区的认定;③有利于完成放疗计划实施前的验证。(三)放射治疗的并发症PLC放射治疗的并发症包括急性期(放疗期间)及放疗后期(4个月内)的肝损伤。1. 急性毒副作用 放疗期间主要的毒副作用包括:①厌食、恶心、呕吐,较严重的有上消化道出血,特别是放射野累及较大体积的十二指肠、空肠和胃的患者;②急性肝功能损害,表现为血清胆红素和ALT上升;③骨髓抑制,特别是在大体积的肝脏受照的患者,或伴脾功能亢进的患者。2. 放射的后期损伤 主要的放射后期损伤是放射诱导的肝病(radiation induced liver disease, RILD)。它的临床表现和诊断标准是:①已接受过肝脏高剂量的放疗;②在放疗结束后发生;③临床表现有两种:典型的RILD发病快,患者在短期内迅速出现大量腹水和肝脏肿大,伴AKP升高到正常值的2倍以上,或ALT上升至正常值的5倍以上;非典型RILD仅有肝脏功能的损伤,AKP升高到正常值2倍以上,或ALT上升至正常值的5倍以上,没有肝脏的肿大和腹水;④能排除肝肿瘤发展、放疗或介入后、药物性肝病或病毒性肝炎活动造成的临床症状和肝功能损害。对RILD的治疗是对症治疗,包括使用肾上腺皮质激素、利尿剂,同时给予积极的保护肝脏的药物和支持疗法。RILD是一种严重的放射并发症,一旦发生,可引起肝功能衰竭,死亡率很高。避免RILD发生的最关键措施是在设计放疗计划时,把正常肝脏受照剂量严格限制在能耐受的范围内。根据我国的资料,肝脏的耐受剂量(全肝平均剂量)在Child-Pugh A级患者可能是23 Gy,Child-Pugh B级患者可能是6 Gy,该结论来自于大分割的放疗,即每次4~6 Gy,每周照射3次,总剂量50 Gy左右。对容易发生RILD的患者更应该小心,包括:原有的肝脏功能差,如肝脏功能为Child-Pugh B;正常肝脏的受照体积大,剂量高;放疗与TACE联合治疗的间隔时间短于1个月。另外,在放疗期间出现急性肝脏功能损伤的患者,如≥RTOG II级肝损伤,对这类患者如果继续放疗,则以后发生RILD的几率可高达60%。因此,对这类患者应该停止放疗,以避免治疗后RILD的出现。急性肝损伤往往可逆、易修复;而后期肝损伤常常不可逆,是严重的放射性损伤,一旦发生,死亡率很高。(四)小结在PLC的治疗中,放疗可以应用于下列情况:①局限于肝内肝细胞癌:放疗与介入联合治疗有可能延缓肝内局部播散,显著提高有效率和生存率,循证医学证据为C级;②肝细胞癌伴癌栓:放疗针对外科或介入治疗后出现的癌栓以及原发灶的癌栓(包括下腔静脉癌栓),可以延长患者生存期,循证医学证据为C级;③肝细胞癌伴淋巴结转移:放疗可显著改善淋巴结转移的肝细胞癌患者的生存期,循证医学证据为C级;④肝细胞癌肾上腺转移:放疗可缓解肾上腺转移灶出现的症状,但尚无证据说明放疗可以延长生存期;⑤肝细胞癌骨转移:放射治疗的目标为缓解症状从而提高患者生存质量,但无证据说明能够延长患者生存期;⑥肝内胆管细胞癌:放疗可延长切除术后切缘残癌和不能切除的肝内胆管细胞癌患者的生存期,循证医学证据为C级。上述PLC的放疗大部分属于姑息性的手段,疗效较差,即使能延长生存期,也仅为数月;但是其它的治疗方法,也未能显示更好的疗效,因此,放疗仍然是可考虑的重要治疗方法之一,特别是针对肝外的转移病灶。八、原发性肝癌的生物治疗与分子靶向治疗国内外已广泛开展PLC的生物治疗,涉及免疫治疗(细胞因子、过继性细胞免疫、单克隆抗体、肿瘤疫苗)、基因治疗、内分泌治疗、干细胞治疗等多个方面。目前,大多数生物治疗方法或技术尚处于研发和临床试验阶段,小部分已应用于临床。一些单中心的小规模临床试验结果提示生物治疗可提高患者的生活质量、减少术后复发率。乙型肝炎相关性HCC患者根治性切除术后长期应用INFα辅助治疗,可以有效地延缓和降低复发率,并具有抗病毒疗效。一般认为,适当应用胸腺肽α1和IL2可以增强免疫功能、辅助抗病毒和抗肿瘤作用,有助于降低术后复发和改善生活质量。国内学者多数报告,细胞因子与其他抗肿瘤治疗联合应用。目前用于肝癌过继性细胞免疫治疗的免疫活性细胞主要是细胞因子诱导的杀伤细胞(CIK)和特异杀伤性T淋巴细胞(CTL)。CIK细胞治疗对于清除残癌、降低抗肿瘤毒副反应、改善生活质量有较好疗效。放射免疫靶向治疗具有一定疗效。我国SFDA已批准131I-美妥昔单抗注射液用于肝癌治疗,需扩大病例,进一步观察,获得更确切的证据,尚不推荐作为常规治疗。肝癌疫苗和基因治疗正在进行临床试验中,其中树突状细胞(DC)疫苗受到较多关注。生物化疗等综合治疗模式显示出良好的效果和耐受性,但缺乏大规模、多中心协作研究的证据。由于生物治疗开展随机对照的大规模临床试验研究难度大,循证医学证据还不充分,不推荐作为常规治疗,但可作为辅助治疗或不能手术情况下的治疗选择。已知PLC的发病机制十分复杂,其发生、发展和转移与多种基因的突变、细胞信号传导通路和新生血管增生异常等密切相关,其中存在着多个关键性环节,正是进行分子靶向治疗的理论基础和重要的潜在靶点。近年来,分子靶向药物治疗肝癌已成为新的研究热点, 受到高度的关注。主要包括:①抗EGFR药物,如埃罗替尼(Erlotinib)和西妥昔单抗(Cetuximab);②抗血管生成药物,如贝伐单抗(Bevacizumab)和Brivanib等;③信号传导通路抑制剂,如mTOR抑制剂依维莫司(Everolimus,RAD001);④多靶点抑制剂,如索拉非尼(Sorafenib)和舒尼替(Sunitinib)等。索拉非尼是一种口服的多靶点、多激酶抑制剂,既可通过抑制血管内皮生长因子受体(VEGFR)和血小板源性生长因子受体(PDGFR)阻断肿瘤血管生成,又可通过阻断Raf/MEK/ERK信号传导通路抑制肿瘤细胞增殖,从而发挥双重抑制、多靶点阻断的抗HCC作用。多项随机、双盲、平行对照的国际多中心III期临床研究表明,索拉非尼能够延缓HCC的进展,明显延长晚期患者生存期。因此,索拉非尼已相继获得欧洲EMEA、美国FDA和我国SFDA的批准,用于治疗不能手术切除和远处转移的HCC;2008版NCCN指南也已经将索拉非尼列为晚期HCC患者的一线治疗药物。至于索拉非尼与其他治疗方法(手术、介入、化疗药物和放疗等)联合应用能否使患者更多地获益,正在进一步临床研究。舒尼替尼也已经开展III期临床研究,有望成为下一个肝癌靶向治疗药物;而其他分子靶向药物及其生物化疗方案的临床试验也在进行。总之,生物治疗,特别是分子靶向治疗在控制HCC的肿瘤增殖、预防和延缓复发转移以及提高患者的生活质量等方面可能具有独特的优势;循证医学高级别证据已充分证明索拉非尼可以延长晚期HCC患者的生存期,而联合其他治疗药物或方法有可能取得更好的效果。九、原发性肝癌的中医药治疗在机体多种恶性肿瘤中,PLC是我国传统医药治疗中最常见到效果的肿瘤之一。中医以整体观念根据患者的全身特点辨证论治,可以适用于各型各期肝癌。曾经有学者收集全国100多种治疗肝癌的单方和验方,发现确实有中药治疗后肿瘤好转甚至消失的,但是多为个案报告,方法流派过多,很难统一。中医中药治疗应注意整体的攻补兼顾,根据肝癌患者的不同情况,采用不同的治则。一般来说,中医药治疗肝癌的优势在于有利于稳定病情,毒副作用轻微、症状改善较明显,使病情发展减慢,少数病人肿瘤缩小或带瘤较长期生存,患者易于接受和费用比较低廉。目前认为中医药可以作为PLC的辅助治疗,有助于减少放、化疗的毒性,改善癌症相关症状,提高生存质量,并且有可能延长生存。我国SFDA已经批准并在国家基本药物目录中纳入了一批现代中药制剂用于治疗肝癌,但存在的问题是早年的研究规范性较差、可重复性不佳和缺乏高级别的循证医学证据。目前正在进行中药制剂治疗肝癌的大规模多中心随机对照研究,值得期待。十、原发性肝癌的系统化疗早在20世纪50年代起,系统性化疗就用于治疗PLC。多数传统的化疗药物,包括阿霉素(ADM)、5-氟脲嘧啶(5-Fu)、顺铂(PDD)和丝裂霉素(MMC)等,都曾经试用来治疗肝癌,但单药有效率都比较低(一般<10%),可重复性差,毒副反应明显,且没有改善生存时间,因此多年来停滞不前,迄今尚无标准的化疗药物或方案。近年来,新一代的细胞毒性药物(如奥沙利铂、卡培他滨、吉西他滨及伊立替康等)相继问世,使得胃肠癌的化疗有了长足的进步,预后显著改善,也推动了对于肝癌系统性化疗的研究。目前认为,对于没有禁忌症的PLC晚期患者,系统化疗优于一般性支持治疗(Best support care, BSC),仍不失为一种可以选择的治疗方法,其主要适应症:(1)合并有肝外转移的晚期患者;(2)虽为局部病变,但不适合手术治疗和肝动脉介入栓塞化疗者;(3)合并门静脉主干癌栓者。上述新一代的细胞毒性药物的临床研究和探索应用,使PLC不适合系统化疗的传统观念正在受到挑战和质疑。一些小样本研究和临床观察提示客观有效率有所提高,可以控制病情发展,减轻症状,可能延长生存,受到重视,但是迫切需要大宗病例随机对照、多中心临床研究的结果来进一步明确,如奥沙利铂为主的联合化疗治疗PLC的国际Ⅲ期临床研究正在进行。由于我国PLC常见高发,大多数患者具有乙肝和肝硬化背景,起病隐袭、进展迅速,确诊时往往已达晚期,不能手术切除或TACE治疗的患者较多,生存期较短和预后极差,有必要去积极探寻高效低毒的新的系统化疗及其与分子靶向药物合理的联合应用。十一、结 语综上所述,PLC是我国的高发肿瘤,治疗难点在于:①大多数患者具有乙肝和肝硬化背景,常合并肝功能障碍;②发病年龄相对较低,进展迅速,容易发生肝内播散和远处转移;③仅部分患者可接受手术治疗,根治性切除率较低;④手术后复发率高。一般认为,影响疗效的重要因素包括肿瘤的大小和数目、肿瘤累及的部位和范围、门静脉癌栓与远处转移、肝功能代偿程度及全身状况。因此,必须重视PLC的早期发现和早期诊断,强调实施规范化综合治疗。首先必须遵循循证医学的基本原则;其次应该广泛深入地开展多学科交流,为PLC患者制定最佳的个体化治疗方案,避免不恰当或者过度治疗;第三,应该把肿瘤生物学基础研究与临床实践经验相结合。此外,专科医疗准入制度的健全和专业医师培训对于PLC的规范化诊断治疗也是非常重要和必须的。由于时间限制,有关研讨会对于肝癌诊断治疗的某些方面未能深入讨论交流,如肝癌局部消融治疗的其他方法、病毒性肝炎相关肝癌患者的抗病毒及其并发症治疗、切除术后辅助治疗等,以及综合应用多种治疗方法针对性的个体化治疗,均有待今后进一步探讨。在对PLC诊疗的实践经验和临床研究进行认真讨论后, 本共识由若干专家执笔写作,虽经反复修改,仍难免局限性,因此,需要不断补充,动态完善。更有必要在上述多学科专家共识的基础上,积极借鉴国际指南和国内外的最新进展,主要依据循证医学的原则制定出符合我国国情的PLC临床指南,那样必将有力地推动PLC规范化诊疗和研究和提高水平,为我国人民和全人类的卫生健康事业作出积极贡献。(杨秉辉、从文铭、周晓军、陈孝平、杨甲梅、樊嘉、王建华、杨仁杰、李槐、蒋国梁、曾昭冲、陈敏华、陈敏山、梁萍、吕明德、罗荣城、刘鲁明、秦叔逵、叶胜龙等参与执笔。肝癌专家共识研讨会和有关工作得到了拜耳先灵医药保健有限公司的大力支持,国际医学信息服务公司(EMD)以及爱思唯尔国际出版集团给予了积极协助,特此致谢!)中国抗癌协会肝癌专业委员会(CSLC)中国抗癌协会临床肿瘤学协作专业委员会(CSCO)中华医学会肝病学分会肝癌学组(叶胜龙、秦叔逵 整理吴孟超、汤钊猷、孙燕、管忠震 审阅)二○○九年二月
周霖 副主任医师 中国人民解放军总医院第五医学中心 介入科2694人已读 - 精选 高强度聚焦超声(HIFU)治疗肝癌的难点与对策
摘要:肝癌的治疗是当前临床医学研究的重点方向之一。大多数肝癌患者确诊时已失去手术切除时机,所以局部治疗就成为这些患者最好的选择。高强度聚焦超声治疗(high intensity focused ultrasound,HIFU)作为一种新的局部治疗方法,以其非侵入性无创治疗、三维适形治疗、可反复治疗及可联合其他局部治疗手段等优势在肝癌的局部治疗中崭露头角。本文将就HIFU治疗肝癌时所面临的难点及其应对方案做一综述。关键词:肝癌;高强度聚焦超声;难点;对策0 引言肝癌是世界上最常见的恶性肿瘤之一,占全部恶性肿瘤的5%以上,全球发病率逐年增长,最近的统计数据表明,肝癌的发病率居全球恶性肿瘤的第5位,病死率居第3位[1]。此病在我国也是高发,当前我国发病人数约占全球的55%;在肿瘤相关死亡中仅次于肺癌,居第二位[2]。大多肝癌确诊时已进展为中晚期,其手术切除率较低,而术后复发率高,术后3年复发率仍高于7O%[3]。因放化疗对肝癌敏感性差,对于无法行手术患者现多应用局部治疗。高强度聚焦超声(high intensity focused ultrasound,HIFU)因其非侵入无创治疗的特点,在肝癌的局部治疗中逐渐脱颖而出。1 HIFU治疗肝癌的原理高强度聚焦超声治疗系统是利用超声波的方向性、组织穿透性和可聚焦性将将集束后的超声波自体外聚焦于体内靶向病灶内,在其焦点处形成高能密度区,使治疗区域内组织发生不可逆性凝固性坏死。其原理主要有:①热效应是指利用超声波的聚焦性使焦点处能量集中,从而产生瞬态高温(达65℃以上),使治疗区域内组织发生凝固性坏死,从而达到对肿瘤的“热切除”;②空化效应 当用高强度聚焦超声辐照组织时,可使其间产生形状不规则的直径约0.02~0.2nm的空化泡,这些空化泡可导致组织内微泡变形,这些微泡发生振动时能释放大量能量从而机械地碎裂组织[4];③机械效应高强度聚焦超声使受到超声作用的组织细胞高速振动,导致细胞发生DNA大分子降解及酶变性等坏死改变。④破坏肿瘤营养血管 恶性肿瘤的生长需要丰富的血供提供营养,HIFU治疗可使为肿瘤提供营养的直径小于0.2mm的血管收缩关闭,形成血栓,从而使肿瘤组织发生缺血坏死[5]。此外,HIFU治疗尚能提高机体对肿瘤的免疫杀伤能力[6],及增强肝癌放、化疗的增敏性。2 HIFU治疗肝癌的适应症与疗效因HIFU治疗是一种非侵入性治疗,对机体影响较小,并且具有三维适形治疗的特性,所以其治疗适应症也较为宽泛。大多数肝癌均可行完全覆盖治疗或姑息性减体积治疗,特别对于肝左叶及尾状叶肿瘤效果更佳。对血供丰富的肝癌可先行肝动脉栓塞治疗,减少瘤体血供后再行治疗。但对于全身状况及心肺功能较差而无法耐受麻醉患者、有严重出血倾向、大量腹水、肝功能严重失代偿伴有重度黄疸者应列为手术禁忌症。HIFU治疗肝癌是确实有效的已得到广泛的认可。经动物实验研究表明,HIFU可从体外有效地使其拟定靶区内的肝组织发生坏死[7]。在临床应用方面也有学者将HIFU治疗肝癌的短期和长期疗效进行比较分析证实了其有效性[8,9]。3 HIFU治疗肝癌的难点因超声波的物理特性、肝脏肿瘤病灶所处解剖位置及其毗邻关系使HIFU治疗过程中面临如下挑战:(1)肿瘤位置被肋骨遮挡HIFU治疗肝癌时,体外超声波需要通过胸腹壁全层以及肿瘤浅面的肝脏组织来传递能量。在这个通路上,肋骨能阻挡超声波的通过,是超声波通路上影响HIFU焦点能量的主要原因,也是导致HIFU消融肝癌效果和效率明显下降的主要原因之一。(2)肿瘤病灶位置靠近膈肌由于肝隔部靠近膈肌并隐藏于右下肺组织的深面,而含气的肺组织不利于超声波能量的传递,且由于肺气及肋骨阻隔、实时监控的超声不能完全显示肝隔顶部及其病灶,这都为HIFU治疗位于膈肌附近肝隔顶的肿瘤带来诸多不便。(3)肿瘤病灶临近特殊部位因肿瘤病灶位于胆囊、肝内胆管、胃肠道、肝门部及大血管附近,在HIFU治疗时因能量传递有可能对上述组织造成损伤,导致出现副损伤或严重并发症。4 应对HIFU治疗时所面临难点的对策4.1 超声通道被肋骨遮挡时的应对方案肝脏肿瘤由于其位置的特殊性,会随呼吸运动而移动,当肿瘤病灶被肋骨遮挡时,可利用肋间隙进行治疗,使HIFU治疗的焦点不正对肋骨,同时结合患者呼吸动度使在肋骨遮挡区内的计划治疗区移动到肋骨遮挡区外,从而实现对靶区域的治疗。这时需要通过控制性呼吸来完成治疗,控制性呼吸是指采用一些措施来控制病人的呼吸动度、暂停呼吸运动和选择性一侧肺通气。目的是使在肋骨遮挡区外的计划治疗区不会移动到肋骨遮挡区、使在肋骨遮挡区内的计划治疗区移动到肋骨遮挡区外。适用于呼气时计划治疗区的头侧治疗部分被遮挡1~1.5cm、吸气时计划治疗区的足侧治疗部分被遮挡1~1.5cm的病灶。但控制呼吸对肺的气体交换的功能有一定的潜在影响,在应用中必须严密监测患者的血氧饱和度,并根据其监测的结果延长或缩短呼吸暂停的时间。必须注意的是对呼吸的控制与HIFU的治疗一定要保持协调一致,否则应立即终止治疗。张卫星等[10]研究表明呼吸控制在全麻下HIFU治疗中应用是安全可靠的。此外,尚可通过切除遮挡肿瘤的肋骨来创造良好的超声通道。肋骨切除的指征:机载显像超声定位,在深吸气和深呼气的情况下,肝肿瘤仍有部分被肋骨遮挡,计划治疗区不能被完全显露,应行肋骨部分切除术,切除遮挡肿瘤的肋骨,以完全显露计划治疗的肿瘤。确定切除肋骨的范围应在机载超声上、完全模拟治疗时的体位进行,并在体表作好切除范围的标记,便于手术中准确切除肋骨。确定肋骨切除范围,除需考虑肿瘤的体表投影和治疗超声的声通道两因素外,还必须考虑手术后软组织的纤维瘢痕收缩所致声通道缩小,故切除肋骨的范围通常应大于超声定位所确定的范围,即通常所说的肋骨切除范围宜大不宜小的原则。但有研究表示肋骨切除尽管能提高HIFU消融肝癌的效果,但肋骨切除并不能改善HIFU治疗中晚期肝癌的疗效及生存率。其临床价值非常有限,因此,肋骨切除适应症应该严格控制,对于不能手术切除的中晚期肝癌不建议行肋骨切除[11,12]。4.2 肿瘤病灶靠近膈肌时的处理临近膈肌的肝癌病灶由于受含气肺组织的遮挡,监控超声常常不能显露或仅能部分显露病灶,一方面给病灶的完全治疗带来了困难,另一方面也增加了肺组织的损伤机会。目前,常采用人工胸水(通过胸腔穿刺人为的有目的向胸腔内注入无菌性生理盐水而造成胸腔积液的方法称之为人工胸水)辅助HIFU治疗肝膈顶部的肿瘤。注入人工胸水后,肋膈角内的含气肺组织被生理盐水推挤而离开,肋膈角内被生理盐水填充,形成良好的超声介质,监控超声就能清晰和完全显示肝膈顶部的病灶,并为治疗超声提供良好的声通道[13]。已有学者[10,14]对人工胸水在HIFU治疗中的安全性进行了研究。此外,行人工胸水时要求肺具有一定的储备功能,在HIFU治疗前一至两周必须进行呼吸功能锻炼,增加心肺功能的储备,提高患者对麻醉及HIFU治疗的耐受性。4.3 特殊部位肿瘤病灶的治疗对策4.3.1肿瘤病灶紧邻重要血管肝门部有丰富的粗大血管,且该处血管血流速度较快,当肿瘤病灶位于此处时给手术切除、射频消融带来很大风险,而肝脏的双重血供系统使动脉介入栓塞的效果大打折扣。在HIFU治疗时,由于超声波在液体中具有最佳穿透性这一特点,肝内外丰富的大血管网络反而成为HIFU治疗的安全保证。因为HIFU治疗时损伤的形成与血管直径和血流速度密切相关。当靶区存在较大血管时,血液流动很快将靶区能量带走,使得HIFU损伤不易形成,从而保证了大血管的安全。伍峰等[15]对164例恶性实体肿瘤患者进行HIFU治疗,其中肝癌68例,研究发现经HIFU治疗后癌灶内滋养血管和毛细血管网大量破坏,肿瘤组织出现缺血性坏死,而靶区内较大血管无损伤或栓塞。有学者报导[16]对39例患者的临近肝脏大静脉的肝癌病灶进行HIFU治疗,术后随访均未发现血管受损。以上研究均说明HIFU可安全地用于治疗毗邻大血管的肝癌。4.3.2肿瘤病灶紧邻胆囊、胆道临近胆管的肝癌在进展过程中常压迫肝内胆管,造成肝内胆道扩张,因胆汁流速较慢,行HIFU治疗时热量易于在胆道沉积从而造成不可逆的胆道损伤。如肝癌病灶与胆囊或肝内粗大胆管临近,行HIFU治疗时除应避开胆道外尚应保留15mm~20mm的安全距离,避免损伤胆道。这是因为在HIFU治疗时治疗靶区能量会向周围扩散,造成治疗计划区域外侧组织热损伤。同时如体内有胆结石、金属植入物、吻合器等高密度异物存在时亦应远离,防止热量在此处沉积,引起周围组织副损伤。4.3.2肿瘤病灶紧邻胃壁 位于肝右叶脏面的肝癌常常紧邻胃壁,在行HIFU治疗时因胃的存在可能产生以下几个方面的影响:胃壁紧贴肿瘤表面,监控超声识别胃壁困难,易造成胃壁的误伤;胃内含有较多气体,影响监控超声对肿瘤的显像、减小HIFU治疗的声通道,缩小了HIFU对邻近胃壁癌灶的治疗范围,同时胃内气体对治疗超声的反射,可引起胃壁损伤。这时可通过胃管向胃腔内注入适量的生理盐水,有利于超声声像识别胃壁,防止胃壁被误伤;同时也增加了监控超声显示的病灶范围和HIFU治疗的超声通道,从而使邻近胃壁的肿瘤灶获得更大的治疗范围并且减少了损伤胃壁的机会。4.4 HIFU治疗作为手术切除前的预处理手术切除仍然是肝癌目前最有效的首选治疗手段,但临床中常因肿瘤体积太大或与血管关系密切而无法手术。这时可充分利用HIFU对血管破坏作用的差异性,可以在完全覆盖性治疗肿瘤时有效的保护邻近较大血管,使得因血管解剖因素所致部分不能接受外科手术的肝癌患者的手术切除成为可能。如果肿瘤体积过大,尚可通过HIFU治疗部分杀灭肿瘤细胞,减小肿瘤负荷,使肝癌降期,提高肝癌的手术切除率。Kennedy等[17]曾对11例肝癌患者先行HIFU治疗,然后进行手术切除,均取得了良好的治疗效果。还可将HIFU治疗作为手术前的预处理,通过术前HIFU治疗使肿瘤病灶坏死,从而减少术中出血、降低手术难度、减少术中因挤压所致肿瘤转移风险。5总结高强度聚焦超声治疗已成为治疗无法手术切除肝癌的重要手段,是今后肝癌综合治疗中一项重要的组成部分。通过进一步完善HIFU治疗,将HIFU与其他治疗方式相结合,特别是加强与手术切除的结合,来加大肝癌的治疗效果、提高肝癌整体的综合治疗水平具有重要的临床价值及广阔的应用前景。目前,国内外尚无大样本、多中心的HIFU治疗和前瞻性的临床随机对照研究,对于HIFU治疗与肝癌转移、复发的关系等问题,尚需进一步开展研究工作,为其更好的临床应用提供有力的依据。参考文献[1]黄洁夫主译.肝胆胰外科学[M].北京:人民卫生出版社,2010:1144.[2]中国抗癌协会肝癌专业委员会.原发性肝癌规范化诊治专家共识[J].临床肿瘤学杂志,2009,14(3):259-269.[3]Kim SH,Lee WJ,Lim HK,et a1.Predicion of viable tumor inhepatocellular carcinoma treated with transcatheter arterial chemoembolization:usefulness of attenuation value measurement at quadruple-phasehelical computed tomography [J].J Comput Assist Tomogr,2007,31(2):198-203.[4]刘春梅,李发琪,王智彪.高强度聚焦超声空化效应的研究进展[J].临床超声医杂志,2007,9(4):233-235.[5]Yang R,Sanghvi NT,Rescorla FJ,et al.Liver cancerablation with extracorporeal high intensity focused ultrasound[J].EurUrol,1993,23:17-23.[6]谢勋鹂,冉立峰,伍烽.H22移植性肝癌高强度聚焦超声治疗后的免疫变化[J].肿瘤学杂志,2008,14(4):254-256.[7]Luo W,Zhou X,Zhang J,et al.Analysis of apoptosis andcell proliferation after high intensity focused ultrasound ablation combinedwith microbubbles in rabbit livers[J].Eur J GastroenterolHepatol,2007,19:962-968.[8]Li YY,Sha WH,Zhou YJ,et al.Short and long termefficacy of high intensity focused ultrasound therapy for advancedhepatocellular carcinoma[J].Gastroenterol Hepatol,2007,22:2148-2154.[9]毕京鹏,周丁华,张建华,等.高强度聚焦超声治疗肝癌的疗效观察[J].中国综合临床,2012,28(5):519-521.[10]张卫星,邓卫萍,黄耀.呼吸控制和人工胸水在肝癌HIFU治疗中的应用[J].中国现代医生,2007,45(6):19-20. [11]金成兵,朱辉,王智彪,等.HIFU联合TACE治疗不能手术切除中晚期肝癌的临床分析[J].中国超声医学杂志,2008, 24(8):741-744.[12]金成兵,朱辉,王智彪,等.肋骨切除术在HIFU联合TACE治疗中晚期肝癌中的临床价值[J].重庆医科大学学报,2009,34(4):475-478.[13]Fukuno H,Tamaki K,Urata M,et al.Influence of an artificial pleuraleffusion technique on cardio-pulmonary function and autonomic activity[J].J MedInvest,2007,54(1-2):48-53.[14]吴刚明,闵苏.全身麻醉下人工液胸辅助高强度聚焦超声治疗肝癌的安全性观察[J]. 中国现代医学杂志.2011,21(2):227-229.[15]Wu F,Chen WZ,Bai J,et a1.Tumor vessel destruction resulting from high-intensityfocused ultrasound in patients with solid malignancies[J].Ultrasound Med Biol,2002,28(4):535-542.[16]L Zhang,H Zhu,C Jin,et al.High-intensity focused ultrasound(HIFU): effective and safe therapy for hepatocellular carcinoma adjacent to majorhepatic veins[J].Eur Radiol,2009,19(2):437-445.[17]Kennedy JE,Wu F,ter Haar GR,et al.High-intensity focused ultrasound for thetreatment of liver tumours[J].Ultrasonics,2004(42):931-935.
周丁华 主任医师 火箭军特色医学中心 肝胆外科5738人已读 - 精选 如何尽早检出“小肝癌”?
单个结节直径小于3cm叫“小肝癌”,恶性程度较低(称为高分化),只在肝脏的原发部位,癌细胞未向周围散布,也未向别处转移。治疗时只要把“小肝癌”手术切除,或“射频消融”(一种介入治疗)可以破坏掉,绝大多数可以根治。但有少数患者会在肝脏的另一部位再次发生,可以再次做相同的治疗。小肝癌恶性程度低,从直径0.5cm长到1cm大概需要4-6个月,甚至更久。那如何尽早检出“小肝癌”?肝癌只发生在肝硬化和慢性肝炎患者中,必须从众多慢性乙型肝炎病毒携带者中检出慢性肝炎,从肝炎和肝硬化患者中检出可疑的肝癌,进一步用CT或磁共振确定诊断。B超如发现小结节、血清甲胎蛋白增高是肝癌的可疑线索,但B超可以漏检、约有1/4的肝癌患者甲胎蛋白正常,所以筛查的方法必须两者并用。根据小肝癌生长速率,由不能检出到能检出的时间,绝大多数在6个月内,当前一般定期每6个月检查B超和甲胎蛋白。对于发生肝癌的高危人群需要密切关注,如“小三阳”肝炎、大于40岁男性、活动性肝硬化、酗酒、近亲患恶性肿瘤(尤其患肝癌)。最好每3-6个月检查B超和甲胎蛋白。
涂上卿 医师 上饶市人民医院 感染性疾病科2781人已读 - 精选 化疗副作用的处理方法
1、恶心和呕吐:恶心和呕吐是化疗副作用中最常见和最可怕的两种。发生频率和严重性因不同的药物和不同的人而有所不同。恶心和呕吐通常发生在化疗后几小时,持续时间不长。持续几天的严重恶心和呕吐并不常见。病人异常恶心,呕吐超过一天,或者恶心得连流质也无法下咽时,一定要告知医生或护士。改变饮食习惯和服用止吐药能减轻这两种症状。不同的止吐药对不同的人有效,因此,在症状减轻前试用几种药是必然的,不要轻易放弃,你应继续同医生一起找出对你最有效的药。大约有一半的化疗病人在化疗前就感到情绪不稳,这叫治疗前恶心。对付治疗前恶心的最好办法是借助于放松技巧。(我们稍后再讨论)。你也可试试以下方法:1)·不要吃得太多,这样你的胃就不会感到太饱。一天中多餐少食。2)·不要在吃饭时喝饮料,必须在饭前或饭后一个小时。3)·吃喝要慢慢进行。4)·不要吃甜的、油炸的或脂肪多的食物。5)·吃冷的或室温下的食物,这样你不会闻到气味难受。6)·慢慢咀嚼食物以助于消化。7)·如果早上感到恶心,那么起床前就吃一些干食品,如麦片、烤面包或饼干。(如果你口腔咽喉疼痛或口干,就不要吃这些东西。)8)·喝冷的、干净的饮料,如苹果汁、茶或放掉气的姜汁啤酒。9)·吮食冰块、薄荷糖或酸的糖果。(如果你口腔咽喉疼痛,就不要吃这些东西。)10)·避免接触使你恶心的气味,如油烟、香烟和香水。11)·饭后坐在椅子上休息,但至少饭后两个小时才能躺下。12)·穿宽松的衣服。13)·感到恶心时,你可慢慢地做深呼吸。14)·你可通过与朋友或家人聊天、听音乐、看电影或电视来分散注意力。15)·采用办法放松一下。· 如果化疗时常常感到恶心,那么至少化疗前几小时不要吃东西。 2、脱发:脱发(秃头症)会破坏人的心情。不是所有的化疗药物都会导致脱发,一些人的头发也只是变得稀疏一点。医生会告诉你的脱发是否由化疗所引起。化疗引起的脱发,在化疗结束后大都会重新长出来。然而,头发的颜色或发质可能会有所不同。毛发脱落发生在身体的各个部位,不仅仅在头部。脸上的毛发、手臂和大腿上的毛、腋毛和阴毛都会受到影响,但是通常不会马上脱落。一般来说,化疗进行一阵以后,毛发才开始脱落。那时,毛发逐渐或成块脱落,残存的毛发也变得干滞无光泽。化疗时,你的头发和头皮需要特别护理,请按以下建议试试:。使用温和的洗发液。。使用软的梳子。。如果必须用吹风,请用低稳一档。。不要用发卷做头。。不要染发或定型。。剪短发。短发使你的头发看上去要浓密一点,即使脱发也易处理。。使用防晒油,戴帽子、围巾或假发来保护头发受太阳照射。。用绸缎枕套。如果你要戴假发,下面有一些窍门:。毛发大量脱落前就去选购假发,这样可以按照自己原来头发的颜色、发质和样式进行挑选。。你可以去专门针对癌症患者的假发店购买。 3、疲劳:疲劳是化疗最常见的副作用之一,轻则精神不振,重则筋疲力尽。疲劳在化疗开始阶段和结束阶段,表现最为严重。象大多数其它副作用一样,化疗一结束,疲劳也会随之消除。在接受化疗期间,以下建议有助于你对付疲劳:*多休息。*与医生一起制订一个锻炼计划。*食物营养要平衡,并喝大量的饮料。*限制你的活动量:只做那些对你很重要的事情。*需要帮助时,不要羞于提出。可请求家人、朋友和邻居帮做一些事情,例如照顾小孩、购物、做家务或开车。*邻居在百货公司购物时,可请他们帮忙顺便买一些东西。*坐久或躺久以后,要慢慢起来,以免头昏眼花。 4、贫血、感染和出血:骨髓生成三种重要的血液成分:给人体细胞输送氧的红血球;抵抗感染的白血球;帮助血液凝结和止血的血小板。化疗会破坏骨髓细胞,从而使产生的血细胞减少。每种血细胞数量的减少,会引起特定的副作用。医生在化疗期间会检查病人的血细胞数量,并给病人服用生长素来帮助骨髓生成新的血细胞。(1)贫血:当红血球太少时,人体组织得不到足够的氧,从而不能正常工作。这种现象叫做贫血,症状表现为疲劳、头昏眼花、脸色苍白、身体发冷,甚至呼吸急促。运用上节“如何对付疲劳”中的办法来解决贫血的症状。同时,把症状告诉医生也很重要。医生在治疗时会经常检查病人的红血球数量。如果你的红血球数降得很低,你就需要输血或用生长素来促进红血球的生长。(2)感染:白血球数量很低的现象叫做白血球减少症,这会降低你抵抗感染的能力。一种嗜中性的白血球对抵抗感染特别重要。嗜中性白血球缺乏的现象叫做嗜中性白血球减少症。感染可能发生在身体的任何部位,但通常是口腔、皮肤、肺、尿道、直肠和生殖器官。如果你的白血球数量下降很多,医生会推迟治疗,降低化疗药物的剂量或采用生长素来提高骨髓生成白血球的数量。采取以下措施来预防感染:*勤于洗手,特别是饭前以及上洗手间前和上洗手间后。*·远离患有感冒、流感、麻疹或水痘等传染病的人。*避免去人多的地方。*远离刚接受小儿麻痹症、麻疹、腮腺炎和风疹等疫苗免疫治疗的小孩。*每次大便后,完全清洁直肠区。如果上火或生痔疮,要看医生后,才能用灌肠剂或栓剂。*不要扯破指甲的表皮。*使用剪刀、针或刀时,小心不要划伤自己。*使用电动剃须刀,不要用刮胡刀,以免划伤皮肤。*使用柔软的牙刷,以免损伤牙龈。*不要挤压或抓搔疙瘩。*每天洗一次温水澡(不要太烫)。轻轻擦干皮肤,不要很用力。*如果皮肤干裂,可使用洗液或油脂。*用温水、肥皂和杀菌剂清洁伤口。*给动物或小孩洗澡时,要戴上手套。*在医生确认前,不要进行免疫注射。当你的白血球数很低时,即使非常小心,你的身体也不能免于被感染。对有可能已被感染的迹象和症状要很注意,并且定期检查身体,对眼睛、鼻、口、生殖和直肠部位要特别注意。受到感染的症状包括:*38℃以上的发烧*发冷*出汗*肠松弛*小便时有灼烧感*严重的咳嗽或咽喉痛*异常的阴道流出物或阴道发痒*伤口、痛处、疙瘩、静脉导尿口或动脉通路口周围发红、肿胀或敏感*腹痛立即把感染的所有迹象都告诉医生。在未经医生许可前,即使你发烧,也不要用阿斯匹林、退热净或其它药物来退烧。(3)出血或凝块问题:化疗药物会影响骨髓生成血小板的能力(血小板通过填塞受损的血管和帮助血液凝结来帮助止血)。如果你的血液中没有足够的血小板,即使受了小伤,你也会比平常更易出血或瘀血。如果你注意到皮肤上有瘀血的小红点、尿液泛淡红、大便发黑有血,你应告诉医生。你也应把牙龈和鼻出血、剧烈头痛、头昏眼花、虚弱加剧或关节肌肉疼痛这些情况告诉医生。医生在你治疗期间会经常检查你的血小板数,如果太低,就需输入血小板。如果你的血小板数很低,为了避免发生问题,可遵循以下建议:*在未经医生许可前,不要服用任何药物,这包括阿斯匹林和其它非处方消炎止痛药。因为其中的某些药会破坏血小板,加重出血问题。*在未经医生许可前,不要喝任何含酒精的饮料。*使用特别柔软的牙刷清洁牙齿。*使用柔软的棉纸轻轻清洁鼻孔。*使用剪刀、针、刀子或其它工具时要小心,不要划伤自己。*熨衣服或做饭时要小心,不要烫伤自己。伸手进烤箱时,要戴隔热手套。*不要从事运动和其它容易受伤的活动。*使用电动剃须刀,而不要使用刮胡刀。 5、口腔:良好的口腔护理在癌症治疗过程中很重要。化疗药物会引起口腔咽喉疼痛、干燥上火或出血。口腔疼痛不仅很痛,而且会被口腔里的细菌引起感染。感染在化疗时很难对付,而且会引起严重问题。因此,采取一切措施来预防它们就显得很重要。以下是一些保持口腔、牙龈和咽喉健康的建议:*化疗前去看牙医,把牙齿清洁一下,并解决牙洞、胧肿、牙龈毛病和假牙不合适等问题。*请医生指导你在化疗时最好的刷牙方式。*找一种日用的含氟牙膏来预防牙齿腐蚀,因为化疗很易使牙齿生洞。*每次饭后,用特别柔软的牙刷轻轻刷牙齿和牙龈。牙刷太硬会损伤柔软的口腔组织。*如果你的牙龈非常敏感,请医生推荐一种特别的牙刷(绒毛或丝带)和牙膏。*每次刷牙后,仔细清洗牙刷,并置于干燥的地方。*避免使用市面上的漱口药,因为它们很多都含有大量的盐和酒精。最好请医生推荐温和的漱口药或加入抗生素的漱口药,用来预防口腔感染。如果你口腔的疼痛加重(口腔炎),你可能需找医生进行治疗。如果疼痛使你无法进食,你可以试试以下办法:*向医生询问解决疼痛的方法,请他们开药来缓解疼痛。*吃冷的食物。热的食物会刺激口腔和咽喉。*选用软的、爽口的食物,例如冰淇淋、婴儿食品、软水果(香蕉和苹果酱)、土豆泥、麦片、五成熟的煮鸡蛋或炒鸡蛋、奶酪、通心粉、奶油蛋糕、布丁和果冻。你也可以把煮好的食物加入汤,放在搅拌器里搅拌,使它们滑口,容易进食。*避免刺激性的酸性食物,如西红柿、柑橘类水果和水果汁(柑橘、柚子和柠檬);辛辣的或太咸的食物;粗糙的或干的食物,如生的蔬菜和烤面包。如果口干使你难于进食,可试以下办法:*询问医生能否使用人造唾液产品来润湿口腔。*多喝水。*吮吸冰块、冰棒或无糖糖果。*咬无糖口香糖。*用黄油、人造黄油、肉汁、调味品或肉汤润湿干的食物。*用水泡脆的干食物。*吃软的汤煮食物。*嘴唇太干,可用唇膏。 6、腹泻:当化疗影响肠道内表层细胞时,可能导致腹泻。如果腹泻持续超过24小时,或伴随疼痛和抽筋,就应该看医生了。情况严重,医生会开止泻药。但不要未经医生许可,服用非处方药。你也可以尝试以下办法来控制腹泻:*少吃多餐。*不吃易引起腹泻和腹痛的含纤维多的食物。含纤维多的食物包括粗面包和麦片、蔬菜、豆类、干果、瓜果、爆米花、新鲜的和变干的水果。相反,吃含纤维少的食物,如精面包、精米、面条、奶油麦片、去皮的水果罐头、酸奶、鸡蛋、去皮的土豆泥或土豆片、蔬菜汤、去皮鸡肉和鱼肉。*避免用咖啡、茶、酒和甜食。*避免吃油炸的、油腻的和辛辣的食物。*如果牛奶和牛奶制品使你腹泻加剧,就不要食用。*除非医生反对,否则多吃含钾丰富的食物,如香蕉、橙子、土豆、桃子和杏仁。*多喝饮料,补充腹泻损失的水分。最好喝牛奶、苹果汁、水、淡茶、肉汤和姜汁啤酒。把它们冷至室温后慢慢喝。喝汽水时先放掉气。如果腹泻严重(一天内拉七、八次),要马上看医生。征询医生意见,是否进食流质食品使肠胃得到休息。感觉好一点后,逐步进食上面所列的含纤维低的食物。由于流质食物的营养满足不了你的需要,因此进食不要超过三四天。如果腹泻不见好转,你需要输液来补充损失的水和营养。 7、便秘:某些人出现便秘是由于化疗;另一些人出现便秘是因为他们相比平常,活动量或营养量减少,或者他们服用了某种止痛药。如果两天以上没解大手,要告知医生。你也许需用泻药或灌肠剂。在未同医生商量之前,特别当你的白血球数或血小板数很低时,不要使用这些办法。你可以尝试以下办法来解决便秘:*多饮用水来松弛肠道。温水和热水特别见效。*多吃含纤维多的食物。这些食物有糙米、麦片、蔬菜、新鲜或晒干的水果、干果和爆米花。*做锻炼。出门散步和做操对解决便秘都有帮助。增加活动量之前,记住同医生商量。 8、神经和肌肉:某些化疗药物会产生外围神经病,一种引起麻刺感和灼烧感及手脚发麻无力的病症。其它与神经相关的症状包括身体丧失平衡感、笨拙、拿东西和扣衣服困难、行走困难、下颚痛、听力丧失、胃痛和便秘。除了影响神经,某些化疗药物也会影响肌肉,使肌肉疲软无力和疼痛。神经和肌肉的功能会受到阻碍,但大多数情况下并不严重。它们通常都很短暂,随着时间也会好转。病人有必要临时停止化疗,马上把神经和肌肉症状告诉医生,一定要把由外围神经痛导致的疼痛告诉医生。小心谨慎和生活常识能帮助你解决神经和肌肉问题。例如,你手指麻木,使用尖锐的、高温的或其它危险的物品时就要非常小心。如果你的平衡感受到影响,行走时就要小心翼翼,并且上下楼梯时使用扶手,浴室里放上垫子。本文系马学真医生授权好大夫在线(www.haodf.com)发布,未经授权请勿转载。
马学真 主任医师 青岛市中心医院 肿瘤科10.7万人已读 - 精选 什么是PET-CT检查?
田耕医生肿瘤科普系列之三 PET/CT的全称叫正电子发射断层显像/X线计算机体层成像。同时提供解剖显像和功能显像,是目前影像诊断技术中最为理想的结合。特别是在肿瘤的诊断、分期、疗效评估等方面发挥重要的作用。那么PET/CT的原理是什么?PET/CT的原理是什么? 为了更好的说明这个问题,从下面这个例子入手可能更好理解:现在有两颗黄豆,一颗是炒熟的,但颜色没变,另一颗没炒,你有什么方法把它们鉴别开吗?图一:你能说出哪一个是炒熟的黄豆吗? 显然,从颜色、形状、大小、质地、轻重等方面无法将它们区分开,但它们是有本质区别的:炒过的黄豆是没有活性的,而没炒的黄豆是有生物活性的,当给予适当的温度和水,它会长成豆芽。因此它们的区别在于是否有活性:图二:炒过的黄豆是没有活性的,是“死”的,而没炒的黄豆是有生物活性的。如果有一种方法能够鉴别是否有活性,就能够将它们区别开。 PET/CT就是这样一种检查,可以检查出不同病灶的代谢活性,从而为鉴别诊断提供重要信息。恶性肿瘤有一个共同的特性就是代谢活性非常高。它是人体内的“强盗”,掠夺性的摄取营养,往往是肿瘤患者越来越瘦,可肿瘤却越长越大。葡萄糖是人体细胞(包括肿瘤细胞)能量的主要来源之一,因此恶性肿瘤摄取的葡萄糖远远多于其它正常组织。利用这一特性,在葡萄糖上标记上带有放射活性的元素氟-18作为显像剂18F-FDG,将此显像剂注入静脉内,在体内循环,恶性肿瘤摄取的18F-FDG远多于其它组织,因此,肿瘤细胞内可积聚大量18F-FDG,经PET显像可以检测到体内18F分布情况从而显示肿瘤的部位、形态、大小、数量及肿瘤内的放射性分布。临床应用举例 一位患者因咳嗽咳痰就诊,痰中查见癌细胞,医生给他做了胸部CT,结果如图三:图三:哪个病灶是癌?两个病灶都是癌? CT看到这位患者左右肺各有一个占位病灶,增强扫描也未能提供足够的信息来判断出每个病灶的性质。于是这个患者的诊断有下列几种可能:1.右肺癌,左肺良性占位病变,如无远处转移,可能需要行右肺手术;2.左肺癌,右肺良性占位病变,可能需要行左肺手术;3.双肺均为癌,则要双肺同时治疗。可见弄清楚诊断是多么重要,错误的诊断意味着错误的治疗。纤维支气管镜和肺穿刺活检是临床常用的方法,但如果能有一种无创、简便的方法将两个病灶鉴别开来该多好。 这位患者做了PET检查,结果如图四:图四:左侧病灶(红色箭头,右肺病灶)是高代谢病灶,考虑为癌。 可以看到图中左侧的病灶(红色箭头,右肺病灶)呈现较深的黑色,表示摄取了较多的18F-FDG,是一个高代谢病灶,考虑为恶性肿瘤;右侧的病灶(蓝色箭头,左肺病灶)颜色很淡,表示摄取18F-FDG不多,是一个低代谢病灶,考虑为良性病变。患者痰中已查到癌细胞,因此,该患者的诊断已经明确:右肺癌,身体其它部位未见转移。最后接受了右肺手术治疗。 肿瘤领域是PET/CT应用最广泛的领域,18F-FDG是目前应用最广泛的显像剂,PET/CT在其它领域也有应用,还有其它多种显像剂应用于不同疾病。PET/CT应用举例下面是一位体检发现癌胚抗原(CEA)升高患者的诊治经过,我对这位患者的病情进行了分析,对如何动态监测肿瘤标志物、如何分析肿瘤标志物升高、发现肿瘤标志物升高后怎么办、PET/CT及各种检查的优缺点等问题进行了分析解答,具有一定的代表性,希望对其他患友有帮助。深圳市第二人民医院肿瘤生物治疗科田耕患者:病情描述(发病时间、主要症状、就诊医院等): 由于头晕住院,病人已很长时间有脑梗、糖尿病、高血压、肾囊肿、动脉硬化等疾病,在住院进行的一系列检查中,有一项“癌胚抗原”偏高,第一次查实17.57,医生怀疑有肿瘤,但多个部位进过CT、彩超等检查都查不到肿瘤,后复查“癌胚抗原”为8.22,医生建议到大医院做PET-CT检查。 长期注射胰岛素,服降压药。 请问是否需要做这个检查?癌胚抗原高是否表示一定会有肿瘤?这个检查能确定肿瘤是恶性还是良性吗?如果要做,哪个医院做最好?费用多少?谢谢!深圳市第二人民医院肿瘤生物治疗科田耕: 您好!在回答是否需要做PET/CT之前,需要详细了解一下病情过程,因为不是所有的标志物升高病人都要做PET/CT: 1.癌胚抗原在正常情况下不应该升高,升高到17.57应引起高度警惕,建议追查; 2.肿瘤标志物应该动态观察,你两次查癌胚抗原的结果差别很大,而且第二次比第一次降低很多,分别是在什么时间查的?是在同一家医院查的吗?哪家医院? 3.已经做过哪几个部位的CT和彩超? 患者:是在同一家医院做的这个检查,就是因为第一次指标太高了,但医生在胸部、肺部、肠道、胃、肝部等都查了,肾和胆、脑部也查了,但我不知道后面这几个检查是不是也是针对肿瘤而做的检查,就是因为查两个部位找不到肿瘤就又查几个部位,到最后哪都找不到时我们家属就要求重新检查那个指标,结果就到了八点多,问过医生为何两次结果会差这么远,他说这是正常现象,因为会有一个峰值的波动,就像血糖一样会有波动。也问过要不要过几天再做一下这个化验,他说没有这个必要,因为两次查都超过了正常值。深圳市第二人民医院肿瘤生物治疗科田耕: 您好!1.这个癌胚抗原结果不常见,特点如下:一、同一家医院检查;二、短期内相差一倍;三、没有经过治疗,第二次就显著降低了。2.血糖会有波动,那是因为吃饭,吃完饭就升高,饥饿时低,与癌胚抗原不同,如果是肿瘤引起的,没有经过治疗,不会出现这么大的波动。3.以下两种方案都可以:一、如经济条件许可,可以直接做PET/CT检查;二、一月后再复查标志物,如仍升高,就做PET/CT检查。4.PET/CT价格约在七千多到一万元,深圳、广州都有,建议到已做过较多病例的医院去做。可以看一下我的文章:肿瘤患者如何使用和分析肿瘤标志物检查 什么是PET-CT检查? PET-CT的两大优点 可能对你有帮助。患者:听了你的建议,我先带父亲重做了CEA,结果仍超出了正常值,为11.5。昨天我带父亲到了深圳武警医院做了PET-CT检查,检查结果说乙状结肠肠壁上块状高代谢病灶,考虑恶性肿瘤可能性大,建议活检确诊。请问这个PET检查能确诊吗?就一定是恶性肿瘤吗?如果是就直接做手术割掉它好了,为什么还要活体检查?如果是恶性肿瘤手术能根治吗?什么方法是最好的治疗手段?深圳市第二人民医院肿瘤生物治疗科田耕: 您好!1.及时的PET-CT检查发现了病灶部位,这是诊断过程的关键一步;2.肿瘤的诊断分很多层次,如影像学诊断、病理诊断等,其中病理诊断就是根据病灶内的细胞来确定疾病的,是最准确的诊断,是诊断的“金标准”,是对疾病的“终审判决”。因此,只要有条件,就应尽可能从病灶上取标本做病理检查,另外,确定了病理诊断,才能根据诊断确定下一步的治疗方案;3.PET-CT是一种功能+影像检查,并不能最终确定肿瘤的诊断,但结和这位患者的资料,肿瘤的诊断可能性非常大。但还有极少数情况是一些非肿瘤性的疾病也可以出现PET-CT检查阳性,因此,要取活检,行病理检查;4.恶性肿瘤的最佳治疗方案是:手术为主的综合治疗;5.恶性肿瘤的治疗效果与多种因素有关,如肿瘤的分期-早期还是晚期?肿瘤的类型?等等,早期的肿瘤疗效好,甚至可以达到“根治”。因此,这位患者及时找到了病灶,为争取好的疗效赢得了时间。祝好!后记:后来这位咨询者在我的患友会里介绍了自己看病及咨询的过程,可能会对标志物升高的患者有一定的启发,转载如下:陪父亲去做这个检查时, 预约好检查的人很多,了解到现在有些有钱的单位其中一项福利就是定期安排职工做这种全身的扫描检查。以前我从来不知道有“PET”这样一种检查仪器,听都没听说过这个东西,所有的了解从网络开始,一开始曾犹豫过要不要带父亲做这个检查,因为当时曾咨询过好几个医生,大都说CEA这个指标其实没有很大的参考意义,一个肿瘤外科医生说CEA是最不可靠的,检查科的主任说根本没有必要去做PET检查,结果为了找到确却的答案我还是带父亲做了这个检查,也就是这个检查告诉我父亲的体内真的有肿瘤,这一刻我既庆幸又难过。我在这里说这些是想告诉别的患者如果有疑虑而经济上又有这个能力的话还是尽早去做这个检查。同时也希望这个检查项目的价格能降下来同时也纳入医保,惠及更多需要他的人。我做了回答:在正确的时间、给正确的患者、选择了正确的检查方法是非常重要的。及时的PET/CT检查发现了病灶部位,这是诊断过程的关键一步。PET/CT在深圳已纳入医保,肿瘤患者可以享受医保。
田耕 主任医师 深圳市第二人民医院 肿瘤科46.1万人已读 - 案例 肝癌晚期HIFU术
治疗前患者为巨块型原发性肝癌,临床症状表现为腹痛,病灶直径超过10cm治疗后治疗后30天复查MRI提示肝癌病灶完全坏死,并缩小,腹痛消失。
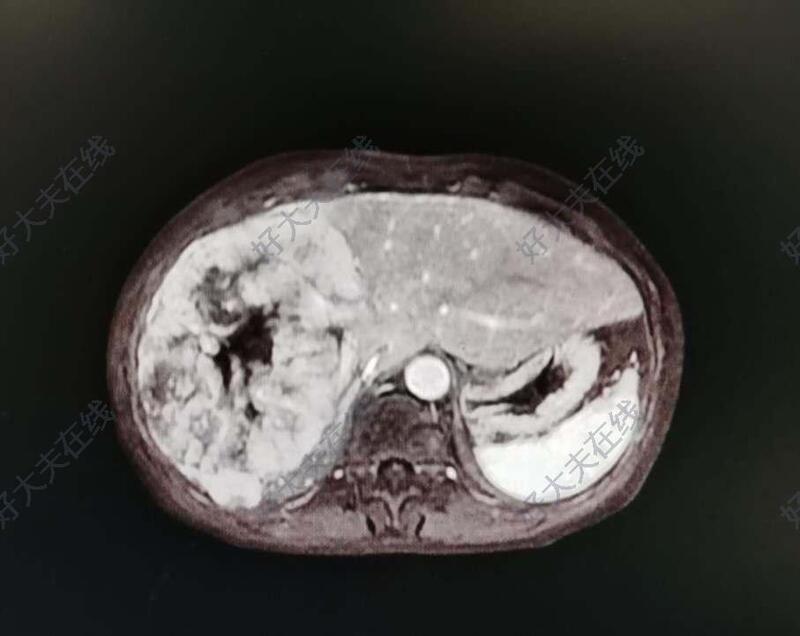 马玉虹 主治医师 重医附二院 肿瘤中心71人已读
马玉虹 主治医师 重医附二院 肿瘤中心71人已读 - 医学科普 输液为什么不用钢针,要选择留置针?
患者通常的疑问主要包括以下几个: 1.钢针输完液后就拔掉了,但是留置针输完后还继续留在血管内,会不会对身体造成影响? 2.现在打钢针的越来越少,是不是你们医院有什么猫腻吧? 3.留置针放在血管里,会不会堵塞血管呢? 先说结论吧:第一,与传统的钢针相比,留置针对血管损伤最小,安全性高,不用担心堵塞血管。 第二,打留置针真的不是因为医院想赚你的钱。 首先说说,为什么淘汰了传统的钢针 钢针进入的血管浅,容易滑出,人没办法活动。 钢针容易刺破血管壁,导致静脉鼓包,引起药物外渗、血管肿胀、静脉炎等。很多人过去都有这样的记忆:打完针好久,手背上还青一大块,就是这个原因。 不容易固定,尤其是小朋友,需要拿一块纸板固定,或者一条又一条的脚步绑着。 孩子好动,钢针滑出之后,又得重新打针,又是一番惊天动地。相信很多妈妈都印象深刻。 钢针在血管内,稍微动一下就容易将血管对穿,扩大血管的损伤,增加痛苦。 钢针对血管的损伤修复缓慢。 再说说,留置针有什么优点呢? 留置针的前端是软管,而不是坚硬的钢针,所以留置针前端的软管漂浮在血管内,可以避免刺破血管,减少对血管的刺激和摩擦,对血管内壁的损害小。 留置针可以任意弯曲,所以容易固定,不易滑脱出来。 留置针可以避免多次打针,尤其是需要打几天针患者,只要打一次就可以了,不用每天都来看着孩子打针哭闹一番。 患者带着留置针可以正常活动,可以洗澡,方便穿衣脱衣。 留置针外渗的几率要远远小于钢针,所以安全性高于钢针。 留置针的软管进入到血管里后,受温度和湿度的作用,会变得更加柔顺,在血管内呈漂浮状态,所以安全时间内不用担心堵塞血管。 美国静脉指南(INS标准) 静脉输液应当选用创伤最小的留置针 留置针能满足输液治疗的需要 留置针穿刺次数最少,留置时间最长,对病人损伤最小 留置针风险小且安全,不推荐使用钢针连接导管、给药装置、外界端口。 国内专家建议 钢针适合于一次性治疗,也就是输液量小、输液时间小于4小时的治疗 钢针容易滑脱,对孩子影响比成人大,并且对孩子血管的损害是不可逆的 静脉留置针可以留置3~5天,避免多次穿刺。 留置针对血管的保护及安全性优于钢针 看完这篇文章,相信你心中的纠结应当化解了吧,下次去医院,您大可以放心了。
马玉虹 主治医师 重医附二院 肿瘤中心4万人已读





